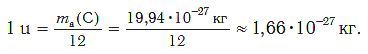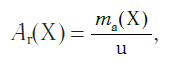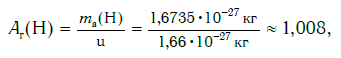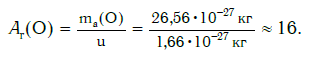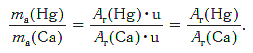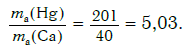Относительная атомная масса
Относительная атомная масса – это масса атома, выраженная в атомных единицах массы (а. е. м.). Относительную атомную массу принято абозначать как Ar. Большинство природных химических элементов представляют собой смесь изотопов, поэтому за относительную атомную массу элемента принимают среднее значение относительной атомной массы природной смеси его изотопов с учетом их содержания в земных условиях. Именно эти значения и приведены в Периодической системе. Например, кислород имеет три изотопа 16 О, 17 О и 18 О, их атомные массы и содержание в природной смеси приведены в таблице 1.
| Изотоп | Содержание в природной смеси, атомн., % ni | Атомная масса изотопа (а.е.м), Ar,i |
| 16 О | 99,759 | 15,995 |
| 17 О | 0,037 | 16,999 |
| 18 О | 0,204 | 17,999 |
Среднее значение атомной массы с учетом вклада каждого изотопа вычисляется по следующей формуле:
Ar = Σ Ar,i × ni, где Ar,i – атомные массы соответствующих изотопов, ni – содержание их в природной смеси (в мольных долях).
Подставляя в эту формулу соответствующие значения из таблицы 1 для атомной массы кислорода, получаем:
Ar = 15,995×0,99759+ 16,999×0,00037 + 17,999×0,0024 = 15,999 а.е.м.
Обратите внимание, что атомная масса и массовое число – совершенно различные понятия: первое – масса атома в а.е.м., а второе – число нуклонов в ядре. Атомная масса – дробная величина (имеет целое значение только для изотопа 12 С), в отличие от массового числа, которое всегда является целым.
Численно эти величины очень близки. Например, для водорода атомная масса равна 1,0078, а массовое число равно 1, для гелия атомная масса равна 4,0026, а массовое число – 4.
Относительные атомные массы имеют дробные значения по следующим причинам:
При образовании любой связи всегда выделяется энергия, на что расходуется часть массы связывающихся частиц. В случае образования химических связей эта величина очень мала, поэтому изменением массы здесь пренебрегают и считают, что масса образовавшейся частицы равна сумме масс частиц, участвующих в ее образовании. При образовании же ядра, выделяется очень большая энергия, и дефект массы хорошо заметен.
Урок 2. Относительная атомная масса химических элементов
В уроке 2 «Относительная атомная масса химических элементов» из курса «Химия для чайников» рассмотрим разные способы выражения массы химических элементов. Напоминаю, что в прошлом уроке «Атомы и химические элементы» мы рассмотрели, кто и когда высказал идею о том, что все вокруг состоит из атомов; также выяснили, что из себя представляет химический элемент и каким образом обозначается.
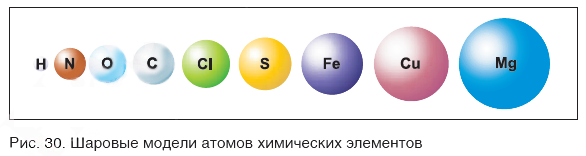
Чем различаются атомы разных элементов между собой? Вы уже знаете: массой, размерами и строением. На рисунке 30 показаны шаровые модели атомов некоторых химических элементов, конечно, не в реальных размерах, а многократно увеличенные. В действительности атомы настолько малы, что их невозможно рассмотреть даже в самые лучшие оптические микроскопы.
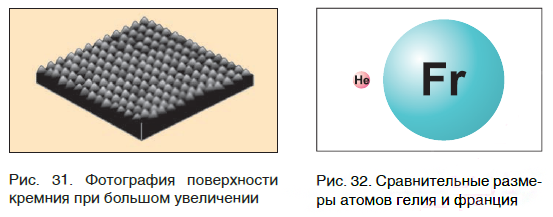
На заметку: В конце XX в. у ученых появились более совершенные микроскопы, позволяющие достигать увеличения в несколько десятков миллионов раз. Они называются туннельными микроскопами. На рисунке 31 показана фотография поверхности кремния. На ней отчетливо видны отдельные атомы, расположенные на поверхности этого вещества.
Размеры и масса атомов
Современная наука обладает методами, позволяющими определять размеры и массы атомов. Так, например, самый легкий атом — атом водорода. Его масса равна 0,0000000000000000000000000016735 кг. Самым маленьким является атом гелия He. Диаметр этого атома равен приблизительно 0,00000000098 м. Записывать и читать такие числа затруднительно, поэтому обычно их представляют в более удобном виде: 1,6735·10 −27 кг и 9,8·10 −10 м. Атомы большинства химических элементов по своим размерам значительно больше атома гелия. Самый большой из них — атом элемента франция Fr. Его диаметр в 7 раз больше диаметра атома гелия (рис. 32).
Еще больше различаются атомы разных элементов по массе. Масса атома обозначается символом ma и выражается в единицах массы СИ (кг). Так, например, масса атома углерода равна: ma(С) = 19,94·10 −27 кг, а атома кислорода — ma(О) = 26,56·10 −27 кг. Масса атома самого тяжелого из существующих на Земле элементов — урана U — почти в 237 раз больше массы атома водорода.
Атомная единица массы
Пользоваться такими маленькими величинами масс атомов при расчетах неудобно. К тому же, когда в XIX в. начало формироваться атомно- молекулярное учение, ученые еще не представляли реальных размеров и масс атомов. Поэтому на практике вместо истинных масс атомов стали применять их относительные значения. Они рассчитывались по массовым отношениям простых веществ в реакциях друг с другом. Химики предположили, что эти отношения пропорциональны массам соответствующих атомов. Именно так в начале XIX в. Дж. Дальтон ввел понятие относительной атомной массы, приняв за единицу сравнения массу самого легкого атома — водорода.
В настоящее время в качестве такой единицы сравнения используется 1/12 часть массы атома углерода (рис. 33). Она получила название атомной единицы массы (а. е. м.). Ее международное обозначение — u (от английского слова «unit» — единица):
Атомная единица массы — это 1/12 часть массы атома углерода, которая равна 1,66·10 −27 кг.
Относительная атомная масса
Сравнивая средние массы атомов различных элементов с атомной единицей массы, получают значения относительных атомных масс химических элементов.
Относительная атомная масса элемента — это физическая величина, которая показывает, во сколько раз масса атома данного химического элемента больше 1/12 части массы атома углерода.
Относительная атомная масса обозначается символами Ar ( А — первая буква английского слова «atomic» —атомный, r — первая буква английского слова «relative», что значит относительный), следовательно:
где Х — символ данного элемента.
Например, относительная атомная масса водорода:
В таблице Менделеева приведены относительные атомные массы всех элементов. В расчетах при решении задач мы будем пользоваться округленными до целых значениями этих величин (см. урок 1).
Внимание! Очень часто относительную атомную массу называют просто атомной массой. Однако следует отличать атомную массу — величину относительную (например, Ar(О) = 16) — от массы атома — величины, выражаемой в единицах массы — килограммах ( ma(O) = 26,56·10 −27 кг) или атомных единицах массы ( ma(O) = 16· u ).
Пример. Во сколько раз атом ртути тяжелее атома кальция?
Решение. Относительные атомные массы элементов равны: Ar(Hg) = 201 и Ar(Ca) = 40.
Масса атома ртути равна: ma(Hg) = Ar(Hg)·u (кг).
Масса атома кальция равна: ma(Са) = Ar(Са)·u (кг).
Другими словами, отношение масс атомов этих элементов равно отношению их относительных атомных масс. Следовательно, отношение масс атомов ртути и кальция равно:
Ответ: в 5,03 раза.
Краткие выводы урока:
Надеюсь урок 2 «Относительная атомная масса химических элементов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Молекулярная физика. Атомная единица массы. Атомная масса.
Атомная единица массы.
Атомная единица массы (а.е.м.) — единица массы, равная 1/12 массы атома изотопа углерода 12 С:
Чтобы перевести значение массы атомов или молекул, выраженной в а.е.м., т. е. относительную молекулярную (или атомную) массу вещества Mr, в единицу массы СИ (кг), пользуются формулой:

Относительная молекулярная масса (атомная масса) — относительное значение массы молекулы (атома), выраженное в атомных единицах массы:

где Mr — относительная молекулярная (атомная) масса; m0 — масса молекулы (атома), выраженная в единицах СИ (кг); m0С — масса молекулы изотопа углерода 12 С, выраженная в тех же единицах, что и m0.

Атомная масса была взята Д. И. Менделеевым за основную характеристику элемента при открытии им периодической системы элементов. Атомная масса — дробная величина, в отличие от массового числа — количества нуклонов в атоме.
Относительная молекулярная масса вещества складывается из относительных атомных масс (а.м.) входящих в молекулу элементов.
Атомные массы всех химических элементов точно измерены.
АТОМНО-МОЛЕКУЛЯРНОЕ УЧЕНИЕ
КОЛИЧЕСТВЕННЫЕ СООТНОШЕНИЯ
Атомная масса
Большинство природных химических элементов представляют собой смесь изотопов. Поэтому за относительную атомную массу элемента принимают среднее значение относительной атомной массы природной смеси его изотопов с учетом их содержания в земных условиях. Именно эти значения и приведены в Периодической системе.
Например, кислород имеет три изотопа 16 О, 17 О и 18 O, их атомные массы и содержание в природной смеси приведены в таблице ниже.
| Изотоп | Содержание в природной смеси, атомн. % ni | Атомная масса изотопа а.е.м. Аr,i |
| 16 О | 99,759 | 15,995 |
| 17 О | 0,037 | 16,999 |
| 18 О | 0,204 | 17,999 |
Среднее значение атомной массы с учетом вклада каждого изотопа вычисляется по следующей формуле:
Подставив в эту формулу соответствующие значения из таблицы для атомной массы кислорода, получим:
Относительные атомные массы имеют дробные значения по следующим причинам:
При образовании любой связи всегда выделяется энергия, на что и расходуется часть массы связывающихся частиц. В случае образования химических связей эта величина очень мала, поэтому изменением массы здесь пренебрегают и считают, что масса образовавшейся частицы равна сумме масс частиц, участвующих в ее образовании. При образовании же ядра выделяется очень большая энергия, и «дефект массы» хорошо заметен.
Молекулярная масса
— масса молекулы, выраженная в а.е.м. Масса молекулы практически равна сумме относительных атомных масс входящих в нее атомов.
Если же вещество состоит не из молекул, а, например, из ионов (NaCl), или является олигомером [(Н2О)n], то относительную молекулярную массу указывают для формульной единицы вещества. Под формульной единицей вещества следует понимать химический состав наименьшего количества данного вещества.
вещества (М) равна отношению массы этого вещества (m) к его количеству (ν):
Прежнее определение: масса одного моля вещества, численно равна его молекулярной массе, но выражается в единицах [г/моль].
Молярная масса и молярный объем
Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональна массе соответствующей структурной единицы, т. е. относительной молекулярной (или атомной) массе данного вещества:
Согласно закону Авогадро одно и то же число молекул любого газа занимает при одинаковых условиях один и тот же объем. С другой стороны, 1 моль любого вещества содержит (по определению) одинаковое число частиц. Отсюда следует, что при определенных температуре и давлении 1 моль любого вещества в газообразном состоянии занимает один и тот же объем. Нетрудно рассчитать, какой объем занимает один моль газа при нормальных условиях, т. е. при нормальном атмосферном давлении (101,325 кПа) и температуре 273 К. Например, экспери-ментально установлено, что масса 1 л кислорода при нормальных условиях равна 1,43 г. Следовательно, объем, занимаемый при тех же условиях одним молем кислорода (32 г), составит 32 : 1,43 = 22,4 л. То же число получим, рассчитав объем одного моля водорода, диоксида углерода и т.д.
Отношение объема, занимаемого веществом, к его количеству называется вещества.
Как следует из изложенного, при нормальных условиях молярный объем любого газа равен 22,4 л/моль (точнее, Vn = 22,414 л/моль). Это утверждение справедливо для такого газа, когда другими видами взаимодействия его молекул между собой, кроме их упругого столкновения, можно пренебречь. Такие газы называются идеальными. Для неидеальных газов, называемых реальными, молярные объемы различны и несколько отличаются от точного значения. Однако в большинстве случаев различие сказывается лишь в четвертой и последующих значащих цифрах.
Молярная масса газа
Для определения относительной молекулярной массы вещества обычно находят численно равную ей молярную массу вещества (в г/моль). Если вещество находится в газообразном состоянии, то его молярная масса может быть найдена с помощью закона Авогадро. По этому закону равные объемы газов, взятых при одинаковой температуре и одинаковом давлении, содержат равное число молекул. Отсюда следует, что массы двух газов, взятых в одинаковых объемах, должны относиться друг к другу, как их молекулярные массы или как численно равные их молярные массы:
Обозначим относительную плотность газа m1/m2 буквой D. Тогда:
равна его плотности по отношению к другому газуу умноженной на молярную массу второго газа.
Часто плотности различных газов определяют по отношению к водороду, как самому легкому из всех газов. Поскольку молярная масса водорода с точностью до сотых равна 2 г/моль, то в этом случае уравнение для расчета молярных масс принимает вид:
Вычисляя, например, по этому уравнению молярную массу диоксида углерода, плотность которого по водороду, как указано выше, равна 22, находим:
Нередко также молярную массу газа вычисляют, исходя из его плотности по воздуху. Хотя воздух представляет собой смесь нескольких газов, все же можно говорить о средней молярной массе воздуха, определенной из плотности воздуха по водороду. Найденная таким путем молярная масса воздуха равна 29 г/моль. Обозначив плотность исследуемого газа по воздуху через D получим следующее уравнение для вычисления молярных масс:
Молярную массу вещества (а следовательно, и его относительную молекулярную массу) можно определить и другим способом, используя понятие о молярном объеме вещества в газообразном состоянии. Для этого находят объем, занимаемый при нормальных условиях определенной массой данного вещества в газообразном состоянии, а затем вычисляют массу 22,4 л этого вещества при тех же условиях. Полученная величина и выражает молярную массу вещества.
Пример: 0,7924 г хлора при 0°С и давлении 101,325 кПа занимают объем, равный 250 мл. Вычислить относительную молекулярную массу хлора. Находим массу хлора, содержащегося в объеме 22,4 л (22400 мл): m = 22400*0,7924/250 ≈ 71 г. Следовательно, молярная масса хлора равна 71 г/моль, а относительная молекулярная масса хлора равна 71.
Измерения объемов газов обычно проводят при условиях, отличных от нормальных. Для приведения объема газа к нормальным условиям можно пользоваться уравнением, объединяющим газовые законы Бойля-Мариотта и Гей-Люссака:
Если объем и давление газа выражены в других единицах измерения, то значение газовой постоянной в уравнении Клапейрона-Менделеева примет другое значение. Оно может быть рассчитано по формуле, вытекающей из объединенного закона газового состояния для моля вещества при нормальных условиях:
Пример: Какое значение газовой постоянной следует взять для расчета параметров газа, взятого при давлении 10 атм в объеме 100 л?
Описанными способами можно определять молярные массы не только газов, но и всех веществ, переходящих при нагревании (без разложения) в газообразное состояние. Для этого навеску исследуемого вещества превращают в пар и измеряют его объем, температуру и давление. Последующие вычисления производят так же, как и при определении молярных масс газов. Молярные массы, определенные этими способами, не вполне точны, потому что рассмотренные газовые законы и уравнение Клапейрона-Менделеева строго справедливы лишь при очень малых давлениях. Более точно молярные массы вычисляют на основании данных анализа вещества.
Доли вещества
Парциальное давление газа
При определении молекулярных масс газов очень часто приходится измерять объем газа, собранного над водой и потому насыщенного водяным паром. Определяя в этом случае давление газа, необходимо вводить поправку на парциальное давление водяного пара. При обычных условиях различные газы смешиваются друг с другом в любых соотношениях. При этом каждый газ, входящий в состав смеси, характеризуется своим парциальным давлением.
— это давление (pi) которое производило бы имеющееся в смеси количество данного газа, если бы оно одно занимало при той же температуре весь объем, занимаемый смесью.
Если не учитывать поправку на давление паров воды, то вместо найденного объема получим:
Ошибка составит 13 мл, т. е. около 2,5%, что можно допустить только при ориентировочных расчетах.
Эквивалент. Количество вещества эквивалентов
Из закона постоянства состава следует, что элементы соединяются друг с другом в строго определенных количественных соотношениях. Поэтому в химии введено понятие эквивалента (слово «эквивалентный» в переводе означает «равноценный»).
называют условные частицы вещества в целое число раз меньшие, чем соответствующие им формульные единицы.
В окислительно-восстановительных реакциях значения эквивалентного числа окислителя и восстановителя определяют по числу электронов, которые принимает 1 формульная единица окислителя или принимает 1 формульная единица восстановителя.
Если известно количество вещества, то количество вещества эквивалентов всегда в число эквивалентности раз больше (или равно) количества вещества:
В практических расчетах наиболее часто пользуются молярной массой эквивалентов.
вещества В называется отношение массы вещества В к его количеству вещества эквивалентов:
Наряду с понятием молярной массы эквивалентов вещества иногда удобно пользоваться понятием объема эквивалентов газообразного вещества В. Данный объем рассчитывается как молярный объем данного газа, деленный на число эквивалентности вещества:
Понятие об эквивалентах, молярных массах эквивалентов и объемах эквивалентов газообразного вещества распространяется также на сложные вещества. Эквивалентом сложного вещества является такое его количество, которое взаимодействует без остатка с одним эквивалентом любого другого вещества. Такой расчет возможен благодаря закону эквивалентов.
Урок+презентация по химии «Город Химтаун» на тему ПС им Д.И.Менделеева (9 класс)
Выбранный для просмотра документ Открытый урок.pptx
Описание презентации по отдельным слайдам:
Добрый день, дорогие друзья!
Добро пожаловать в Химтаун!
Жители этого удивительного города – Элементики
Весь мир большой- Жара и стужа – Планет круженье, свет зари Все то, что видим, мы снаружи Законом связано внутри Найдется ль правило такое, Что целый мир объединит. Таблицу Менделеев строит, Природы ищет алфавит.
Станция №1 «Домашнее задание»
Станция №2. «Географическая»
Станция №3 «Верю не верю»
Ребята, вам предлагаются пять утверждений о внутреннем строении атома. Вы вправе верить им или нет. Ваша задача в тетради напротив номера утверждения, с которым вы согласны, поставить значок «+», а где не согласны «-».
Станция №4 «Анатомическая»
Вопрос 2 Атом состоит из ……, находящегося в центре атома, и ……. движущихся около него. Атом состоит из ядра, находящегося в центре атома, и электронов, движущихся около него.
Вопрос 7 Число электронов, как и протонов, в атоме химического элемента равно …… …… химического элемента. Число электронов, как и протонов, в атоме химического элемента равно порядковому номеру химического элемента.
Вопрос 14 На первом энергетическом уровне максимально может быть …. электрона. На первом энергетическом уровне максимально может быть два электрона.
Вопрос 15 На втором энергетическом уровне максимально может быть …. электронов. На втором энергетическом уровне максимально может быть восемь электронов.
Вопрос 16 Общее количество энергетических уровней в атоме равно номеру ……, в котором находится элемент. Общее количество энергетических уровней в атоме равно номеру периода, в котором находится элемент.
Вопрос 17 В периоде происходит ….. заполнение орбиталей электронами. Каждый новый период начинается с заполнения электронами ….. энергетического уровня. В периоде происходит постепенное заполнение орбиталей электронами. Каждый новый период начинается с заполнения электронами нового энергетического уровня
Вопрос 20 Периодический закон был сформулирован … …. …. в …. году. Периодический закон был сформулирован Дмитрием Ивановичем Менделеевым в 1869 году.
Вопрос 21 Формулировки периодического закона: свойства элементов и их соединений находятся в периодической зависимости от …. …. (Д.И. Менделеев), от …. ….. (современная). Формулировки периодического закона: свойства элементов и их соединений находятся в периодической зависимости от массы атома (Д.И. Менделеев), от заряда ядра (современная).
Станция №6 «Характеристическая»
Спасибо за внимание
Выбранный для просмотра документ Урок-путешествие.docx
Урок – путешествие « Город Химтаун»
Тема: Характеристика химических элементов по положению в периодической системе химических элементов и строению атома.
Цель урока: раскрыть роль Периодического закона как фундаментального закона природы; закрепить умения и навыки характеризовать элементы по их положению в периодической системе и строению атома.
Тип урока: усвоения знаний, умений и навыков.
Формы роботы: выполнение тренировочных интерактивных упражнений, групповая работа.
Оборудование: Периодическая система химических элементов Д.И. Менделеева, таблица электроотрицательности, таблица «Электронное строение атома» (интернет), алгоритм характеристики химических элементов по положению в периодической системе.
Планет круженье, свет зари
Все то, что видим, мы снаружи
Законом связано внутри
Найдется ль правило такое,
Что целый мир объединит.
Таблицу Менделеев строит,
Природы ищет алфавит.
Станция №1 «Домашнее задание»
1 команда. Он бежит по проводам,
Он бывает тут и там.
Свет зажег, нагрел утюг
Если в атом он попал
То, считай, совсем пропал:
Он с утра и до утра
Носится вокруг ядра. (электрон)
С массою внушительной,
А таких, как он, отряд
Создает в ядре заряд.
Лучший друг его нейтрон.
3 команда. Зарядом я похвастать не могу,
А потому сижу в ядре:
А то подумают: шпион,
А я нейтральный, я … (нейтрон)
Станция №2. «Географическая»
Для путешествия по этому городу мы должны вспомнить географию города и некоторые его координаты (выбираем гида)
-Кто главный архитектор города? (Д.И.Менделеев)
-Сколько улиц в этом городе? (7, 3 малые и 4 большие)
-Сколько домов? (8, нумерация этажей ведется не так как у нас, а наоборот – 1 этаж самый верхний)
-Почему Дмитрий Иванович расселил жителей именно в таком порядке? (с увеличение их атомных масс, чем тяжелее Элементик, тем ниже он живет.Также для того, чтобы жители жили мирно и не ссорились в каждом доме живут соседи с одинаковыми характерами и нравами и по диагонали в соседних домах)
-Сколько жителей в этом городе? (110, всех их зовут Элементики, а фамилии у всех разные)
-В каком районе города живут жители с металлическими характерами? (Металлический характер жителей усиливается справа на лево,). Расскажите, что вы о них знаете?
-А где живет самый активный житель с металлическим характером?(В домах металлические свойства усиливаются сверху вниз).
-В каком районе города живут жители с неметаллическими характерами? (Неметаллический характер ослабевает слева на право). Расскажите, что вы о них знаете?
-А где живет самый активный житель с неметаллическим характером?(В домах неметаллические свойства усиливаются снизу вверх).
Учитель: Молодцы, ребята! Вы хорошо знаете географию города, а его жители оказались в трудной ситуации, и просят нас о помощи. Многие жители плохо знают своих соседей и просят нас рассказать о них. Укажите стрелкой в карте путешествия ослабление металлических и усиление неметаллических свойств в пятерках элементов. Объяснить, на каком основании расставлены стрелки.
1. Как различаются атомы металлов и неметаллов по способностям присоединять и отдавать электроны? (металлы – легко отдают электроны, а неметаллы принимают)
Станция №3 « Верю не верю»
Ребята, вам предлагаются пять утверждений о внутреннем строении атома. Вы вправе верить им или нет. Ваша задача в тетради напротив номера утверждения, с которым вы согласны, поставить значок «+», а где не согласны «-».
1.Только электроны входят в состав атома.
3.Количество нейтронов и электронов одинаковое.
4.Относительная атомная масса равна количеству электронов.
5.Заряд ядра зависит от количества протонов.
А теперь поменяйтесь тетрадями с соседом. Внимание на экран (Слайд 4). На нём появились ответы. Сверьтесь и оцените работу. Количество правильных ответов совпадает с оценкой.
Объясните, почему высказывания 1, 3 и 4 неверны? (С места 1 – 2 ученика)
Станция №4 «Анатомическая»
Что вы знаете о строении атома?
Отвечаем на вопросы (презентация оранжевая)
Вставьте пропущенные слова.
Место химического элемента в периодической системе определяется количеством ____________ в ядре атома
3. Ядро имеет ___________________ заряд и состоит из
________________ и __________________.
4. Сумма чисел протонов и нейтронов соответствует
5. Изотопами называют разновидности атомов с одинаковым количеством _________________, но разным количеством ___________________ в ядре атома.
6.Свойства химических элементов определяются числом ___________, находящихся на ___________________ ___________________________________
С помощью Интернет – паутины мы посетим кабинет доктора Всезнайкина, который знает об анатомии все. А вы можете похвастаться такими знаниями?
Доктор Всезнайкин даже по строению анонимного больного может определить его фамилию и адрес по которому он проживает. А вы можете? (заходим на интернет-сайт http://www.xumuk.ru/esa/ и с помощью таблицы «Электронное строение атома» проверяем умение и навыки построения электронных уровней элементов).
Станция№ 5 «Развлекательная»
Ребята! А вы заметили, что за нами наблюдают жители внеземной цивилизации и они немного заскучали? Давайте их развлечем и загадаем им несколько загадок. Посмотрим, также хорошо знают этот город во всей Вселенной, как и на нашей планете Земля. ( Загадки на презентации и фокусы)
Отгадываю задуманный элемент. Описание игры. Ведущий просит одного из учеников задумать любой химический элемент по периодической системе. После этого ведущий предлагает провести с номером этого элемента следующие вычисления без сообщения промежуточных результатов:
а) номер элемента удвоить;
б) к произведению прибавить 5;
в) сумму умножить на 5.
Последний результат сообщается ведущему, который тотчас объявляет задуманный играющим элемент.
Объяснение игры: разгадка заключается в следующем: пусть задуман элемент № 25 (марганец). Проведем с числом 25 соответствующие математические действия:
25 2 =50; 50 + 5 = 55; 55 5 = 275.
Сегодня 1-й день работы нового почтальона этого города, он еще не познакомился с жителями и столкнулся с такой проблемой: забывчивые отправители писем не написали фамилии адресантов и мы должны ему помочь по электронному строению элемента указать его имя и адрес.
Станция №7 «Характеристическая»
Главным итогом жизни Менделеева стала периодическая система химических элементов.
И каждый взмах ее взлетев
Суровым гением своим
Повеял миру Менделеев
В природе понятое им…
Учитель: Вот мы и в гостях у местных жителей. Но, их так много! (Вопрос: сколько химических элементов известно к настоящему времени?). Некоторые из них такие активные, быстрые, суетливые, что вносят неразбериху в четкую и размеренную жизнь страны. Придется помогать: объяснять их свойства и возможности. Задание № 1: охарактеризуйте элемент № 16 по плану:
Вам необходимо дать характеристику элементу с данным порядковым номером. На подготовку дается 3 минуты (план характеристики элемента на экране и у каждой команды на столе в карте путешествия).
По истечении времени листочки с ответами сдаются экспертной комиссии.
Учитель: Ну вот, ребята, и закончилось наше путешествие в удивительную страну маленьких Элементиков Химтаун. Я очень надеюсь, что вам было интересно путешествовать по этой удивительной стране. Кто-то повторил выученный материал, а кто-то узнал новое и интересное. Богини путешествий проверят ваши карты путешествий и выставят вам соответствующие баллы, по которым я выставлю вам оценки.
А сейчас запишите домашнее задание : предложите свои примеры действенности периодического закона в окружающем мире.