Атрофический вагинит: лечение

Атрофический вагинит: симптомы
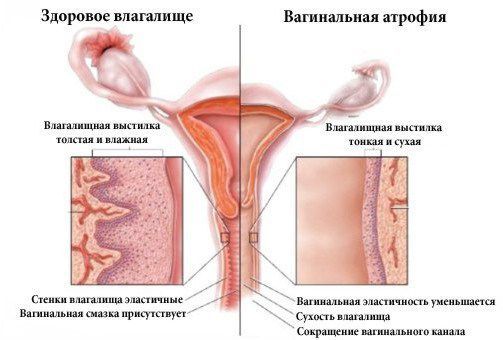
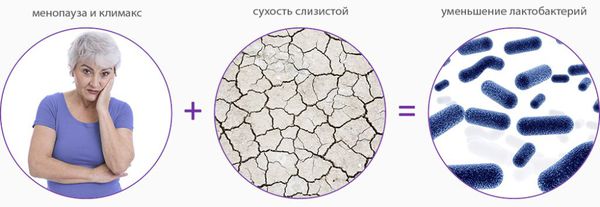
Атрофический вагинит — это комплекс патологических состояний стенок влагалища, таких как воспаление, иссушение и истончение из-за недостатка гормона эстрогена.
Первым беспокойным звоночком станет появление сухости, жжения или зуда. А также снижение сексуального влечения, боли во время секса, кровянистые выделения и учащенные позывы в туалет. Часто при болезни снижается количество смазки или она вовсе пропадает.
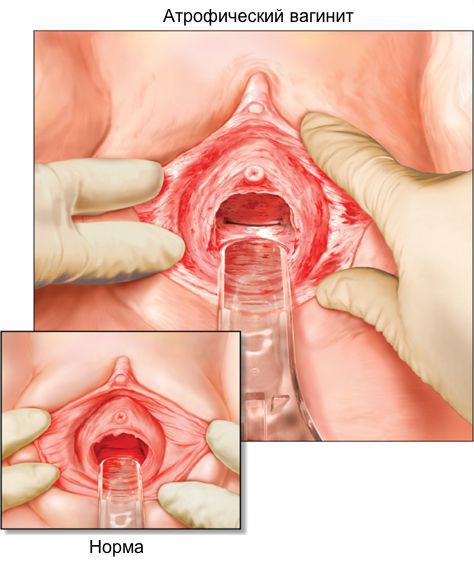
При визуальном осмотре можно заметить, что стенки влагалища сухие и тонкие, слизистая сглаженная (иногда беловатого оттенка), а любой контакт может вызывать кровоточивость. Также возможен спаечный процесс. Впрочем, в некоторых исключительных случаях заболевание протекает вообще без выраженных симптомов.
Если вы обнаружили у себя один или несколько вышеуказанных симптомов, не нужно сразу обвинять партнера в измене, так как заразиться атрофическим вагинитом невозможно. Он не передается ни половым, ни каким-либо другим путем. Главная причина появления болезни — нехватка гормона эстрогена.
Если какой-то симптом вы обнаружили у себя, первым делом нужно обратиться к гинекологу, не допуская самостоятельного лечения атрофического вагинита. Только врач сможет правильно определить болезнь и назначить грамотное лечение.
 Атрофический вульвовагинит: причины появления
Атрофический вульвовагинит: причины появления
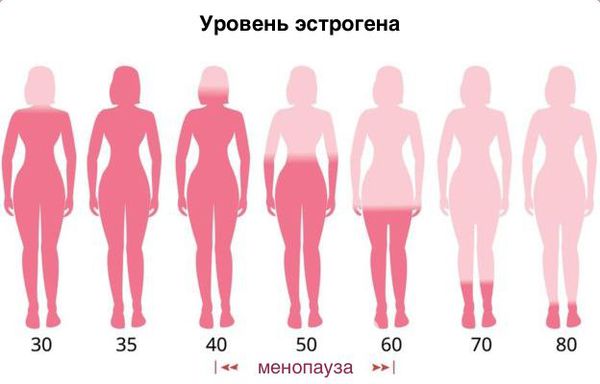
В основном атрофический вульвовагинит проявляется у женщин примерно через 5–6 лет после начала менопаузы. Связано это с тем, что после прекращения месячных у женщин снижается производство эстрогена, из-за чего снижается естественная защита от инфекций.
Кстати, уровень эстрогена может снизиться и по какой-либо другой причине:
постоянный стресс, депрессивное состояние;
употребление некоторых медицинских препаратов;
лучевая терапия органов в тазовой области;
кормление грудью, послеродовой период;
 Как лечить атрофический вагинит
Как лечить атрофический вагинит
К счастью, атрофия слизистой в гинекологии — не приговор, она уже давно успешно лечится. Сегодня самым современным и оптимальным методом считается вульво-вагинальное омоложение с помощью лазера: этим способом воспользовались уже тысячи женщин. Отзывы довольных пациенток, которых больше не беспокоят неприятные симптомы этого заболевания, являются лучшим подтверждением в пользу лазерного омоложения.
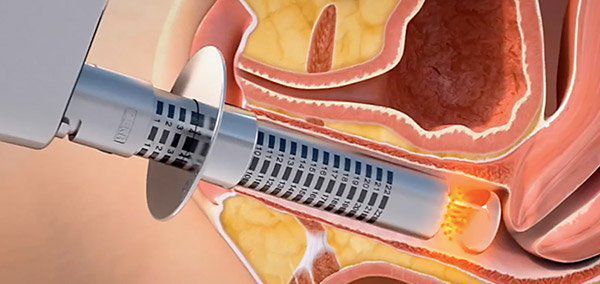
«Лазерный Доктор» — первое в Санкт-Петербурге медико-косметологическое учреждение, в которой стали проводить вульво-вагинальное омоложение лазерной системой SmartXide DOT-2(Италия). В клинике используется специально разработанная методика интимного омоложения MonaLisa Touch, благодаря которой операция проводится эффективно, безболезненно и деликатно. Достигается это использованием специальной насадки, которая отражает лазерные лучи непосредственно на стенки влагалища. Врач, постепенно проворачивая насадку, обрабатывает все 360°.
При этом оказывается двойной эффект: лазер обрабатывает поверхность слизистой, а RF-энергия прогревает подслизистый слой. Глубина проникновения не превышает 4мм, что гарантирует безопасность и безболезненность процедуры. Вся процедура занимает примерно 15 минут.
Чаще всего врачи для избавления от атрофического вагинита советуют именно лазерное интимное омоложение, так как этот метод считается наиболее оптимальным: он эффективный, безболезненный и почти не имеет восстановительного периода. В отличие, например, от хирургического вмешательства или лечения таблетками либо гормонами.
Лечение атрофического вульвовагинита в Санкт-Петербурге
В клинике «Лазерный Доктор» вы можете записаться на прием к опытному врачу-лазеротерапевту и проконсультироваться по всем вопросам, касающимся атрофического вагинита и процедуры лечения. На приеме врач осмотрит состояние эпителия, а также определит наличие или отсутствие противопоказаний. В случае, если их не обнаружится, можно будет сразу записаться на процедуру лазерного интимного омоложения, предоставив необходимые анализы:
УЗИ органов малого таза или заключение от врача-гинеколога об отсутствии онкологии.
Вагинальная атрофия: этиологические аспекты и современные подходы к терапии
Вагинальная атрофия – симптом постменопаузы, характеризующийся эстрогендефицитным состоянием у женщин. Урогенитальный тракт особенно чувствителен к снижению уровня эстрогенов. 27–55% всех женщин в постменопаузе испытывают симптомы, связанные с урогенитальной атрофией (уга), затрагивающей половую функцию и качество жизни.
В клинической картине урогенитальных расстройств в климактерическом периоде выделяют симптомы, связанные с вагинальной атрофией, а также расстройства с мочеиспусканием (цистоуретральная атрофия). Если вазомоторные симптомы проходят со временем, признаки вагинальной атрофии прогрессируют. У 40–57% женщин отмечается сухость влагалища, жжение и зуд, диспареуния, кровотечения, недержание мочи, инфекции органов малого таза.
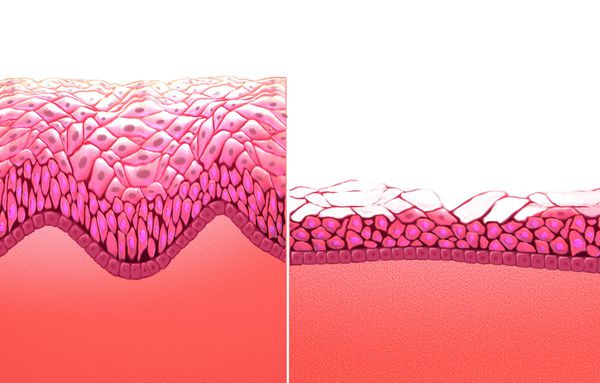
Стенки влагалища состоят из трех слоев: внутреннего, среднего мышечного и наружного соединительнотканного. Атрофические процессы захватывают мышечные и соединительнотканные структуры, а также мышцы тазового дна, уретры, мочевого пузыря. Особенно выражены они в слизистой влагалища, которая состоит из 4 основных слоев эпителиальных клеток: базального, парабазального (митотически активного), промежуточного гликогенсодержащего и поверхностного слущивающегося. Эстрогеновые рецепторы в основном располагаются в базальном и парабазальном слоях и практически отсутствуют в промежуточном и поверхностном. Дефицит эстрогенов блокирует митотическую активность базального и парабазального слоев эпителия, пролиферацию влагалищного эпителия. Следствием прекращения пролиферативных процессов являются исчезновение гликогена – питательной среды для лактобактерий, полное выведение лактобацилл, которые играют ключевую роль в предотвращении заболеваний урогенитального тракта. Вследствие расщепления гликогена при условии достаточного количества эстрогенов образуется молочная кислота, обеспечивающая кислую среду в пределах колебаний РН от 3,8 до 4,4. Подобный механизм приводит к подавлению роста патогенных и условно-патогенных бактерий. В период постменопаузы слизистая оболочка утрачивает защитные свойства, истончается, легко травмируется с последующим инфицированием.
Атрофия слизистой вульвы и влагалища характеризуется истончением, уменьшением вагинальной складчатости, побледнением, наличием петехиальных кровоизлияний, признаков воспаления, а также происходит потеря упругости тканей, подкожно-жировой клетчатки, выпадение лобковых волос, снижение секреторной активности бартолиниевых желез. Как правило, врачи диагностируют вагинальную атрофию на основании сочетания клинических симптомов, визуального осмотра и субъективных жалоб пациентки.
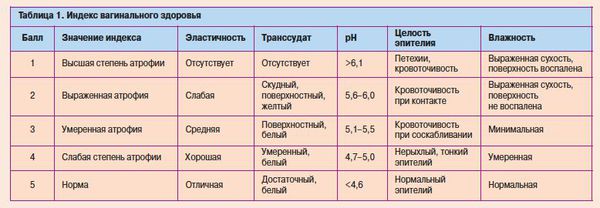
Для диагностики и оценки эффективности лечения вагинальной атрофии необходимо: РН и подсчет вагинального индекса созревания (ВИС, преобладание клеток базального и парабазального слоев), мультистероидный профиль крови.
ЭСТРОГЕНЫ
Эстрогены являются главными регуляторами физиологических процессов во влагалище. Все клинические рекомендации по лечению урогенитальной атрофии сходны в том, что наиболее эффективным методом лечения вагинальной атрофии является локальная гормональная терапия эстрогенами. Для лечения урогенитальной атрофии, сочетающейся с симптомами климактерия, используют системную гормональную терапию. Исследования показали, что локальная терапия устраняет симптомы вагинальной атрофии в 80–90% случаев, а системная терапия – в 75%. Ультранизкие дозы эстрогенсодержащих препаратов обладают выраженным кольпотропным эффектом. Учитывая слабое пролиферативное действие на эндометрий при использовании эстрогена, дополнительного введения прогестагена не требуется.
Роль дефицита эстрогенов у женщины в патогенезе урогенитальных расстройств в период менопаузы ни у кого не вызывает сомнений. Однако клиническая картина климактерического синдрома характеризуется широкой вариабельностью проявлений, поэтому не все урогенитальные расстройства в перименопаузе и постменопаузе могут быть объяснены недостаточным эффектом эстрогенов. С возрастом у женщин происходит значительное снижение уровня как эстрогенов, так и андрогенов. Так, уровень общего и свободного тестостерона, андростендиона и дегидроэпиандростерона в 45-летнем возрасте составляет в среднем 45%, в 60-летнем – около 30%, в 70-летнем – 10% от уровня этих гормонов у 20-летних женщин. Дефицит андрогенов, которому у женщин практически не уделяется внимания, оказывает негативное влияние на все органы и системы организма, особенно на половую систему. Применение ультранизких доз локальных эстрогенсодержащих препаратов является безопасным и эффективным подходом к предотвращению и лечению вагинальной атрофии, не имеет ограничений по возрасту и длительности применения.
АНДРОГЕНЫ
Андрогены у женщин, как и у мужчин, представлены дегидроэпиандростерона сульфатом (ДГЭА-С), дегидроэпиандростероном (ДГЭА), андростендионом, тестостероном и 5α дегидротестостероном (5-α-ДГТ). Однако в отличие от мужчин концентрация первых трех гормонов у женщин выше, чем концентрация двух последних. Секреция андрогенов в надпочечниках регулируется адренокортикотропным гормоном (АКТГ), в яичниках – лютеинезирующим гормоном (ЛГ). У женщин около 25% андрогенов образуется в яичниках, 25% – в надпочечниках, остальные синтезируются в периферических тканях. После наступления менопаузы основным местом синтеза андрогенов становятся яичники. Циркулирующий в крови тестостерон у женщин функционирует как прогормон, способный к конверсии в 5-α-ДГТ или 17-β-эстрадиол в тканях-мишенях.
Андрогеновые рецепторы широко представлены в головном мозге, в изобилии – в женской мочеполовой системе, хотя влияние андрогенов на состояние влагалища изучено недостаточно. Слизистая оболочка влагалища во время возбуждения выделяет муцин и вагинальный транссудат (эстрогензависимая функция), секреция которых у женщин является андрогензависимой. Известно также, что уровень эстрогенов в крови влияет на экспрессию андрогеновых рецепторов во влагалище: у женщин, получающих препараты эстрогенов, плотность андрогеновых рецепторов оказывается ниже, чем у тех, кто такие препараты не получает. При этом показано, что плотность андрогеновых рецепторов в менопаузе существенно уменьшается. Следовательно, уменьшение плотности андрогеновых рецепторов у женщин в постменопаузе в сочетании с возрастным снижением уровня андрогенов в сыворотке крови у них может быть причиной уменьшения андроген-чувствительности тканей влагалища.
Кроме того, в женской половой системе наряду с эстрогензависимыми эффектами регуляции регионарного кровообращения выявлена андрогензависимая NO-опосредованная вазодилатация. Таким образом, уровень эстрогенов у женщин является основным, но не единственным механизмом, обеспечивающим рост клеток гладкой мускулатуры влагалища, а также регулирующим метаболизм соединительной ткани и синтез оксида азота. При дефиците эстрогенов происходит истончение эпителия влагалища, что делает его восприимчивым к травмам и инфекциям. Однако вагинальный эпителий у женщин, которым вводили тестостерон или ингибиторы ароматазы, также демонстрировал увеличение числа слоев клеток, их толщины и числа митозов.
Андрогены усливают экспрессию NO-синтазы в проксимальном отделе влагалища, что проявляется в облегчении релаксации гладких мышц влагалища. Эстрогены, с другой стороны, снижают активность NO-синтазы и повышают активность L-аргиназы, что может привести к относительному дефициту оксида азота и ослаблению релаксации вагинальной ткани. Таким образом, можно предположить, что при нормальном уровне эстрогенов имеющаяся у женщины диспареуния может быть проявлением дефицита вазомиорелаксирующего влияния андрогенов на мочеполовую систему, мионейроваскулярной недостаточностью и спазмом мышц тазового дна на фоне дефицита андрогенов.
Возрастное снижение уровня андрогенов у женщин коррелирует с развитием симптоматики цистоуретральной и вагинальной атрофии. В мышцах тазового дна и нижних мочевых путях имеется огромное количество андрогеновых рецепторов, что делает эти группы мышц также высокочувствительными к анаболическим эффектам андрогенов у женщин. Несмотря на то, что эстрогензаместительная терапия оказывает выраженное положительное влияние на клинические проявления урогенитальных расстройств, у 30–40% системная заместительная гормональная терапия (ЗГТ) не эффективна, поэтому обычно назначают местную терапию эстриолом, основным биологическим эффектом которого является трофическое воздействие на нижние отделы урогенитального тракта. Однако даже при таком подходе у значительного числа пациенток проблемы сохраняются.
СОВРЕМЕННОЕ ВИДЕНИЕ
Зарубежные и российские исследования показывают, что применение тестостерона в постменопаузе может быть эффективным средством лечения вагинальной атрофии, никтурии, недержания мочи как на фоне системной и локальной ЗГТ, так и без нее. Необходим индивидуальный подход к лечению урогенитальных расстройств, учитывающий разные типы течения пери- и менопаузы. Так, пациентки с клинически и лабораторно (мультистероидный профиль, определяемый масс-спектральным методом) подтвержденным дефицитом андрогенов не должны получать препарат ЗГТ с антиандрогенными свойствами, в связи с тем что ряд жалоб, обусловленных дефицитом эстрогенов, могут только усугубиться. В то время как при сохраненной секреции андрогенов назначение препаратов с андрогенной активностью может привести к нежелательным явлениям андрогенизации: спровоцировать рост волос на лице, прибавку мышечной массы, повысить сальность кожи, чрезмерно повысить либидо. Поэтому при выборе препаратов для лечения урогенитальной атрофии учитываются индивидуальные особенности каждой конкретной пациентки, основываясь на показателях ее гормонального профиля.
Ряд экспериментальных исследований показали эффективность применения андрогенных препаратов –
ДГЭА и тестостерона у пациенток в постменопаузе с сексуальными нарушениями и урогенитальными расстройствами. Андрогенные препараты для лечения вагинальной атрофии применяются в качестве эффективных и безопасных средств в виде трансдермального геля тестостерона пропионата, перорального тестостерона ундеканоата интравагинального геля дегидроэпиандростерона (DHEA) – 0,25% (3,25 мг), 0,5% (6,5 мг) и 10% (13 мг). Крем с 0,5% DHEA оказался самым оптимальным для лечения вагинальной атрофии, он эффективен и существенно не влияет на сывороточный уровень эстрогенов.
Помимо перечисленных выше методов лечения вагинальной атрофии, на сегодняшний день существуют такие, как терапия препаратами эстриола с низкими и ультранизкими дозами (0,3 мг и менее 0,1 мг) в сочетании с лактобактериями, селективными модуляторами эстрогеновых рецепторов (оспемифен), а также терапия комбинацией конъюгированных эстрогенов и базедоксифена – селективного модулятора эстрогеновых рецепторов, известной как тканевой селективный эстрогенный комплекс (TSEC), эффективный в соотношении 20 мг/ 0,625 мг.
Таким образом, местная терапия имеет ряд преимуществ перед системным введением препаратов, позволяет избежать первичного метаболизма в лечении, максимально воздействует на эндометрий, имеет низкую гормональную нагрузку, минимальные побочные эффекты, не требует добавления прогестагенов, оказывает в основном локальный эффект. Учитывая патогенез вагинальной атрофии (дефицит не только эстрогенов, но и андрогенов, влияющих на качество мышечной ткани малого таза, сократительную способность мочевого пузыря) рекомендована также терапия с применением интравагинальных гелей (дегидроэпиандростерона), селективных тканевых эстрогеновых комплексов, селективных модуляторов эстрогеновых рецепторов и негормональных методов лечения, а также комбинированных препаратов, содержащих
ультранизкодозированный эстриол и лактобактерин.
Несмотря на то что эффективность лечения высока, не стоит забывать о профилактике заболевания: сохранение регулярной половой жизни очень важно в период менопаузы. При половом акте улучшается циркуляция крови, а семенная жидкость содержит половые стероиды, простагландины и незаменимые жирные кислоты, способствующие сохранению вагинальной ткани.
Что такое атрофический кольпит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Лантухова Э. С., гинеколога со стажем в 14 лет.
Определение болезни. Причины заболевания
Атрофический кольпит (вагинальная атрофия, генитоуринарный синдром) — это состояние влагалища, которое характеризуется атрофическими изменениями (истончением слизистой, сухостью, нарушением защитных функций тканей), и связано с дефицитом воздействия эстрогенов и других гормонов на слизистые. Чаще всего возникает в менопаузе.
Основная причина развития генитоуринарного синдрома — возрастное снижение эстрогенов в пре- и постменопаузе. Схожие симптомы могут испытывать женщины репродуктивного возраста по следующим причинам:
Симптомы атрофического кольпита
Самый ранний симптом недостаточности эстрогенов — снижение увлажнённости влагалища, замечаемое при половом акте. Другие частые симптомы атрофического кольпита (вагинальной атрофии):
Симптомами атрофического цистоуретрита (эстрогендефицитных атрофических изменений в уретре и мочевом пузыре) являются:
Симптомы атрофического цистоуретрита могут быть изолированными или сочетаться с недержанием мочи при напряжении.
Патогенез атрофического кольпита
В основе развития атрофических изменений при данном заболевании лежит изменение гормонального фона.
Дефицит эстрогенов блокирует деление эпителиальных клеток стенки влагалища, в результате чего угнетается клеточная пролиферация (увеличение числа клеток и рост ткани) и образование гликогена — питательной среды для лактобактерий. Это приводит к почти полному исчезновению этих бактерий и нарушениям влагалищного микробиома, так как именно кисломолочные бактерии поддерживают оптимальный уровень pH и подавляют рост патогенной и условно-патогенной флоры. В дальнейшем изменение баланса микроорганизмов ведёт к развитию воспалительных процессов.
Поскольку рецепторы к эстрогенам содержатся в эндотелии сосудов (сосудистой стенке) и нервных клетках, при заболевании снижается кровообращение, развивается ишемия тканей, появляются симптомы жжения, зуда и боли.
В связи с единым эмбриональным происхождением мочеполовой системы данные изменения затрагивают не только влагалище, но и уретру, мочевой пузырь, мышцы и связки тазового дна.
Классификация и стадии развития атрофического кольпита
Различают три степени тяжести урогенитальных расстройств:
Осложнения атрофического кольпита
При отсутствии лечения генитоуринального синдрома возможно развитие выраженных изменений. К осложнениям заболевания относятся:
Диагностика атрофического кольпита
К объективной диагностике атрофического вагинита относятся:
При урологических симптомах проводят общий анализ мочи, посевы мочи, УЗИ почек и мочевого пузыря, КУДИ (комплексное уродинамическое исследование), консультацию уролога. Для исключения кожных заболеваний при необходимости требуется консультация дерматолога.
Лечение атрофического кольпита
При наличии воспаления на фоне атрофии первым этапом проводится санация (устранение возбудителя инфекции), а затем — мероприятия по восстановлению микрофлоры и слизистой.
Лечение симптомов атрофии должно быть дифференцированным и индивидуальным.
Урогенитальные расстройства являются независимым показанием к назначению гормональной терапии. Лучше всего атрофические изменения нивелируют эстрогены для местного применения (эстриол). Препараты эстриола для местного применения имеют минимальную системную абсорбцию (концентрация в плазме не превышает 20 пг/мл), а положительный эффект наступает быстро — через 2-3 недели. При этом у гормональной терапии не выявлено негативного влияния на эндометрий при длительном наблюдении (от 6 до 24 месяцев).
К новым методам лечения умеренной и тяжёлой диспареунии относится одобренный FDA селективный модулятор эстрогеновых рецепторов — оспемифен для приема внутрь, но он имеет ряд противопоказаний и побочных действий.
С целью лечения недержания мочи могут быть использованы инъекции препаратов на основе гиалуроновой кислоты. Востребована и биоревитализация гиалуроной кислотой, в результате которой происходит увлажнение слизистой оболочки, повышение тонуса мышц, усиление либидо. Данные методики имеют временный эффект, так как с течением времени происходит расщепление гиалуроновой кислоты ферментом нашего организма.
Эффективно применение собственной плазмы крови человека, то есть тромбоцитарной аутологичной плазмы — биологического стимулятора процессов регенерации.
Особой популярностью в настоящее время в профилактике и лечении вагинальной атрофии, недержании мочи и опущения стенок влагалища пользуются лазерные технологии (интимный лазерный фототермолиз).
Методика безопасна, безболезненна, имеет короткий курс реабилитации, проводится амбулаторно. В результате происходит улучшение состояния кожи и тонуса мышц, слизистая оболочка восстанавливает эластичность и натуральную лубрикацию, увеличивается её толщина и мягкость за счёт процессов неоколлагенеза и новой васкуляризации.
Прогноз. Профилактика
При выраженных нарушениях (III-IV степени выпадения половых органов, когда опущение выходит за пределы половой щели, появлении изъязвлений, пролежней, свищей, сращений слизистой, а также при отсутствии желаемого результата от консервативной терапии) проводится хирургическое лечение, однако оно в некоторых случаях может быть не полностью эффективным, иметь рецидивы и осложнения. Для улучшения прогноза на этапах подготовки к оперативным вмешательствам и после операции проводится консервативная гормональная терапия.
Профилактика развития генитоуринарного синдрома основывается на систематических осмотрах и своевременном назначении гормональной заместительной терапии после наступления менопаузы.
Клетки эпителия
Плоскоклеточная метаплазия
Процесс, который характеризуется нераковыми изменениями в эпителиальных клетках шейки матки. Плоскоклеточная метаплазия возникает в результате совокупности общих и местных факторов, которые негативно влияют на организм, вызывая обратимый процесс, в ходе которого дифференцированные эпителиальные клетки преобразуются в более выносливые клетки многослойного плоского эпителия, с ороговением или без. Плоскоклеточная метаплазия цервикального канала также возникает как результат слияния с находящимся рядом эндоцервиксом. Изменение типа клеток может приводить к снижению функции эпителия. Когда патологические раздражители устраняются, метапластические клетки приобретают свою первоначальную форму и функцию. Сохранение физиологических стрессоров в областях, подверженных метаплазии, может приводить к дисплазии или предраковым клеточным изменениям. Развитие метаплазированных клеток происходит под влиянием герпеса или бактериальных инфекций (хламидиоз, токсоплазмоз, уреаплазмоз), протекающих на фоне ослабленного иммунитета и имеющих хроническую форму.
Кератоз
Представляет собой патологический процесс, который характеризуется пролиферацией и ороговением клеток плоского эпителия, выстилающего влагалищную часть шейки матки. При этом образуются утолщения или бляшки белого цвета с четкими границами, выступающие над поверхностью слизистых оболочек и могут быть видимы невооруженным глазом до любой обработки растворами.
Гиперкератоз
Это усиленное ороговение верхнего слоя многослойного плоского эпителия шейки матки. Считается, что причиной может быть недостаток эстрогена в организме женщины. В процессе ороговения слизистая покрывается плотными белесоватыми структурами, слегка выступающими над поверхностью здоровой ткани.
Паракератоз
Нарушения Ороговения эпителиального слоя эпидермиса (неполное ороговение). Характеризуется ороговением слизистых оболочек, потерей эпидермисом способности синтезировать кератогиалин (предшественник кератина) и нарушением морфологии слизистой оболочки. При данном процессе пораженный участок цервикального канала выглядит сморщенным из-за нарушения эластичности ткани. Такие островки более грубые.
Опасность представляет лейкоплакия, возникшая в результате активизации вируса папилломы человека высокого канцерогенного риска.
Трубная метаплазия
Характеризуется наличием в строме шейки матки нормальных по строению желез, выстланных клетками, напоминающими эпителий маточной трубы. Данная патология обычно представлена одиночной железой или группой желез и может быть реснитчатая либо секреторная. Трубная метаплазия часто встречается в неупорядоченном пролиферативном эндометрии
Атрофические изменения
Атрофия матки и шейки в большинстве случаев диагностируется у женщин в климактерическом периоде. Результатом данной патологии становится регресс эпителиальной ткани. Однако женщины детородного возраста также не застрахованы от атрофии шейки матки. Заболевание может развиться при дефиците эстрогенов, после оперативных вмешательств на шейке матки, при системных патологиях соединительной ткани. Атрофия шейки матки – один из факторов, вызывающих женское бесплодие.
В основном атрофические изменения происходят в период менопаузы. Снижение выработки гормонов приводит к исчезновению слизистой секреции, изменению бактериальной флоры. В результате происходит поэтапное сокращение толщины эпителия, что приводит ткани к раздражениям, травмам.
Изменения при беременности
В течение беременности устанавливается типичная для данного процесса картина мазка. Эти изменения связаны с продукцией гормонов плацентой и могут быть неверно трактованы как предопухолевые или опухолевые. Реактивные изменения шейки матки связаны с нарушением клеток ее эпителия. Возникают при: воспалениях, гиперкератозе, паракератозе, дискератозе, плоскоклеточной метаплазии, железистой гиперплазии, полипах, лимфоцитарном (фолликулярном) цервиците.
 Атрофический вульвовагинит: причины появления
Атрофический вульвовагинит: причины появления Как лечить атрофический вагинит
Как лечить атрофический вагинит