Что такое эндометрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Делеске И. А., гинеколога со стажем в 8 лет.
Определение болезни. Причины заболевания
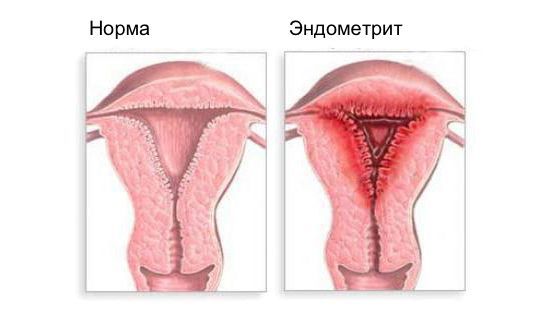
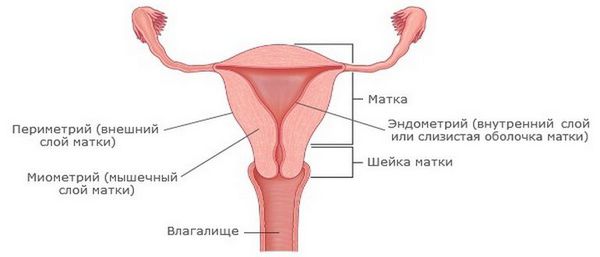
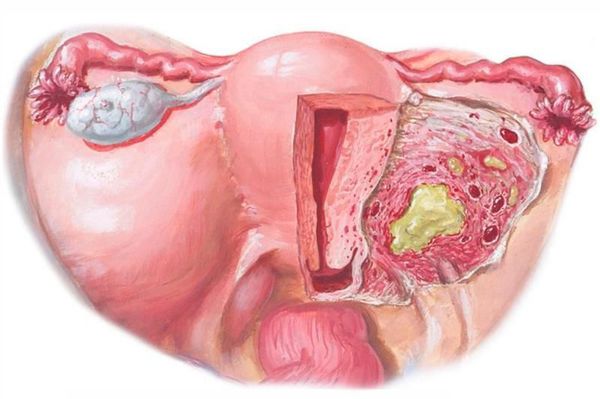
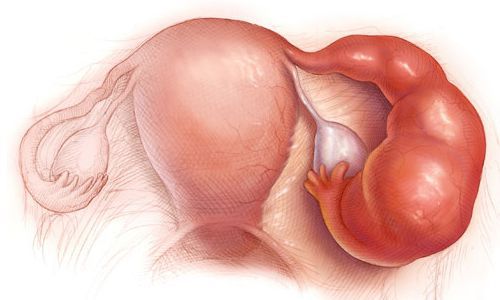
Эндометрит — это воспаление внутреннего слоя матки (эндометрия), которое приводит к изменению его функций. Возникает в результате заражения этой области микробами, вирусами и грибковыми инфекциями.
В женском репродуктивном тракте присутствуют различные микроорганизмы, среди которых преобладают Lactobacillus spp. Эндометрит чаще ассоциирован с чрезмерным размножением бактерий Enterobacter, Enterococcus, Streptococcus, Staphylococcus, Ureaplasma, Mycoplasma.
Эндометрит вызывают также вирусные инфекционные агенты: вирус герпеса, цитомегаловирус, вирус папилломы человека, энтеровирусы и аденовирусы.
Риск развития эндометрита увеличивают:
Симптомы эндометрита
Воспаление может протекать в острой и хронической форме. Чаще всего симптомы эндометрита появляются на четвёртый день после инфицирования. При острой форме эндометрита отмечаются общие симптомы воспаления, такие как слабость, быстрая утомляемость, повышение температуры тела, изменения в общем анализе крови (сдвиг лейкоцитарной формулы влево и повышение СОЭ).
К локальным симптомам острого эндометрита можно отнести:
При отсутствии правильного и своевременного лечения эндометрита в течении 10 дней возможен переход в хронический воспалительный процесс. При этом держится повышенная температура, появляются новые симптомы:
Течение острого послеродового эндометрита более тяжёлое, проявляется в следующих симптомах:
Патогенез эндометрита
На начальном этапе воспаления инфекционный агент (бактерии, вирусы или грибки) внедряется в слизистую оболочку матки. Начинается выработка медиаторов воспаления, которая приводит к нарушению микроциркуляции крови в его очаге. Миграция лейкоцитов в зону повреждения, активация нейтрафилов и макрофагов ведёт к активной выработке цитокинов и перекиси водорода, запуску перекисного окисления липидов с повреждением мембран клеток. В это время на фоне повышенной выработки цитокинов и факторов роста происходит деградация матрикса клеток. Нарушение микроциркуляции крови приводит к развитию локальной ишемии и гипоксии ткани, которые затем активируют процессы склерозирования. При длительной стимуляции иммунной системы происходит её истощение и появление аутоиммунных реакций.
При длительности воспалительного процесса более 2 месяцев можно расценивать его как хронический процесс. Развиваются изменения в структуре и функции ткани, происходит нарушение пролиферации (деления клеток) и физиологической циклической трансформации эндометрия. В связи с этим возможно нарушение нормальной имплантации эмбриона при беременности.
Классификация и стадии развития эндометрита
Эндометрит можно разделить на острую и хроническую форму.
Острый эндометрит возникает при абортах, диагностических манипуляциях, выскабливании, развивается быстро, воспаление сопровождается острыми или ноющими болями и повышением температуры. Наиболее частый путь инфекции при нём — восходящий. Распространение инфекции из влагалища в верхние отделы репродуктивного тракта происходит при несостоятельности барьера шейки матки. Воспаление может локализоваться в эндометрии, а также переходить на миометрий. При несвоевременном и неполноценном лечении возможно развитие пельвиоперитонита (воспаление оболочки брюшины в области малого таза).
Отдельно выделяется острый послеродовый эндометрит — начинается на 2-4 сутки после родов, ему может предшествовать хориоамнионит (инфицирование оболочек плода и жидкости).
При хроническом эндометрите симптоматика сглажена. Характерны периодические обострения и рецидивы после переохлаждения и воспаления другой локализации урогенитального тракта.
По клиническим проявлениям эндометрит подразделяется на клиничеcки выраженную и субклиническую форму.
По характеру воспалительного процесса эндометрит можно разделить на:
По морфологическим признакам:
Осложнения эндометрита
Осложнения у эндометрита могут быть достаточно серьёзными.
Пельвиоперитонит — воспаление выходит за пределы матки, в процесс вовлекаются листки брюшины. Пациентки отмечают резкое повышение температуры, симптомы интоксикации, тошноту, рвоту, интенсивные боли внизу живота (основная локализация ниже пупка), симптом раздражения брюшины ( резкое усиление боли в животе при быстром надавливании и снятии руки).
Диагностика эндометрита
Диагностика хронического эндометрита должна быть основана на комплексном подходе анализа жалоб пациентки, анамнеза, симптомов, результатов эхографических исследований, лабораторной диагностики, данных морфологического исследования эндометрия и иммунного статуса.
Критериями хронического эндометрита является наличие очаговых или диффузных лимфоидных инфильтратов, склероз стенок спиральных артерий, фиброз стромы и наличие плазматических клеток. При этом к абсолютным признакам хронического эндометрита относят плазматические клетки.
Микробиологические посевы используются для выявления возбудителя воспалительного процесса.
При эхографии (УЗИ) хронический эндометрит определяют по:
При гистероскопии определяются следующие признаки хронического эндометрита: гиперемия слизистой оболочки матки, неровномерная толщина эндометрия, полипообразные образования, кровоизлияния, очаговая гиперплазия эндометрия.
Лечение эндометрита
Контрольные критерии эффективности терапии хронического эндометрита:
Прогноз. Профилактика
При своевременном и полноценном лечении прогноз благоприятный. Пациентки отмечают улучшение состояния в течении двух суток. При запоздалом лечении эндометрита возможно развитие септического шока.
Для профилактики эндометрита рекомендуется:
Всё о кровотечениях после менопаузы
Поделиться:
Менопауза — это самая последняя менструация в жизни женщины. Эту точку на длинной дороге жизни врачи обычно определяют ретроспективно — 12 месяцев не было кровянистых выделений, значит, та самая менструация и была точкой менопаузы. Средний возраст достижения менопаузы в нашей стране — 52 года. У кого-то это происходит раньше, у кого-то позже.
Иногда вступление в этот сложный период сопровождается неприятными изменениями характера кровотечений. То скудно, то обильно; то часто, то редко. Не всегда легко понять, нормальны ли эти изменения. О том, как и почему это происходит, мы подробно рассказывали в статье «Нарушения цикла после 40 лет».
На пороге менопаузы стоит бить тревогу и обращаться к врачу за помощью, если:
Однако в постменопаузе любые кровянистые выделение — повод для срочного визита к специалисту. Даже незначительные кровомазания через год и более после последней менструации могут робко свидетельствовать о существующем неблагополучии.
Почему это происходит?
Вот список самых распространенных причин:
Полипы. Как правило, это доброкачественные образования, вырастающие в полости матки. Полип может довольно плотно прикрепляться к стенке матки или расти на самой поверхности эндометрия, держась буквально «на соплях». Иногда у полипа настолько длинная ножка, что позволяет ему «выглядывать» из шейки матки. В таких случаях гинеколог видит полип при обычном осмотре на кресле. Хотя, справедливости ради, гораздо чаще мы видим невооруженным глазом полипы, которые растут из шейки, а не из полости матки.
Атрофия эндометрия. В глубокой постменопаузе из-за крайне низкого уровня женских половых гормонов эндометрий может стать совсем тонким и хрупким. Это совсем не опасно, кровянистые выделения обычно скудные и не представляют угрозы.
Гиперплазия эндометрия. Эндометрий стал слишком толстым. Мы подробно рассказывали об этом заболевании, но в постменопаузе это всегда особенно тревожная история. Особенно если сначала началось кровотечение, а потом мы увидели при проведении УЗИ гиперплазию.
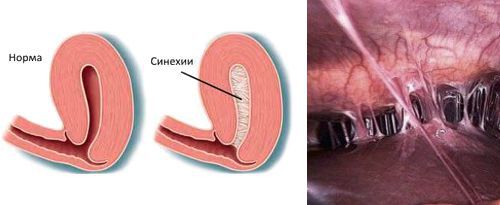
Синехии полости матки. Синехии — это сращения. Из-за выраженной атрофии эндометрия матка «слиплась». В постменопаузе — вариант нормы, но врачи часто очень беспокоятся и суетятся, опасаясь пропустить серьезную проблему. В случае синехий кровянистые выделения обычно невелики, а УЗ-картина может выглядеть страшно и напоминать сильнейшую гиперплазию.
Рак эндометрия. К сожалению, это самая частая причина кровотечений в постменопаузе. Хорошая новость в том, что рак эндометрия сообщает о себе очень рано, когда есть прекрасные возможности для радикального лечения. Если не сидеть в обнимку с боровой маткой и красной щеткой пару лет, прогноз вполне позитивный.
Рак шейки матки. Если мы поставили диагноз «рак шейки матки» только тогда, когда женщина обратилась с кровотечениями в постменопаузе, это очень-очень поздно. Зато если сдавать цитологические мазки с шейки матки (с 21 года) и делать тест на ВПЧ (с 25–30 лет) хотя бы каждые 3–5 лет, мы никогда не пропустим это заболевание. Рак шейки матки около 10 лет «сидит» на предстадиях, когда помочь очень легко. Запущенный рак, который уже проявляет себя кровотечениями из распадающейся шейки, практически неизлечим.
Ставим диагноз правильно
Каждая пациентка с кровотечением в постменопаузе прямым ходом отправляется к гинекологу. После беседы с уточнением деталей, изучением лекарственного анамнеза (привет самолечению БАДами и фитоэстрогенами) доктор проводит осмотр на кресле. Обычно это позволяет понять, откуда течет кровь: травма во влагалище, проблема с шейкой или все-таки кровь вытекает через шейку из полости матки.
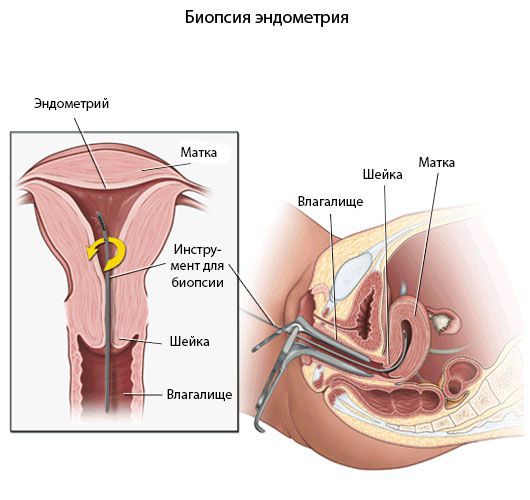
Биопсия эндометрия — специальный инструмент, толщиной со стержень для шариковой ручки, вводится в полость матки для получения кусочков эндометрия. Простая и практически безболезненная процедура, не требующая ни госпитализации, ни обезболивания, ни серьезной подготовки.
Трансвагинальное УЗИ — самый простой и быстрый способ сориентироваться в ситуации.
Жидкостная соногистерография — введение небольшого количества жидкости в полость матки с последующим проведением УЗИ помогает разобраться в сомнительных ситуациях «полип или не полип?».
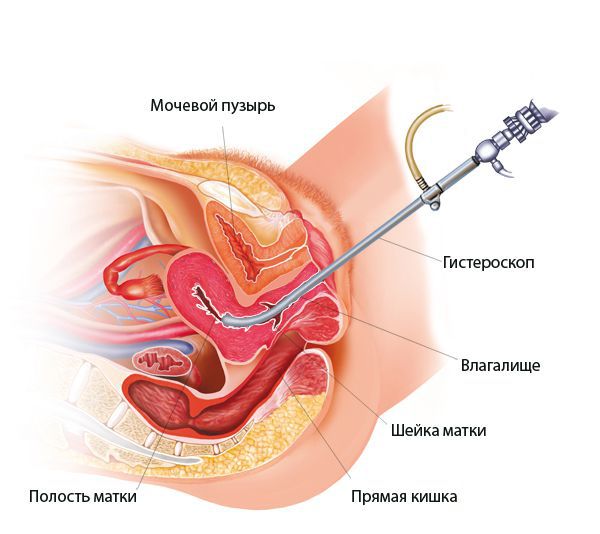
Гистероскопия — метод, позволяющий заглянуть в полость матки. Офисные гистероскопы — тонкие и гибкие — позволяют уточнить ситуацию амбулаторно и даже взять небольшие фрагменты тканей для биопсии под контролем зрения. Это высокоинформативный способ диагностики, особенно при сомнительных результатах ультразвукового исследования. Для удаления полипов или других, более серьезных лечебных вмешательств понадобится гистерорезектоскоп — аппарат покрупнее, который вводят в полость матки после расширения шейки под наркозом.
Выскабливание полости матки — способ остановить кровотечение и получить материал для гистологического исследования. Проводится в гинекологическом стационаре под наркозом. Альтернативой может служить мануальная вакуум-аспирация содержимого полости матки, которую выполняют амбулаторно. Выбор метода зависит от оснащенности клиники, тяжести состояния пациентки, сопутствующей патологии.
Как лечиться будем?
Выбор метода лечения зависит от того, какой поставлен диагноз. Полипы в постменопаузе удаляются с обязательным гистологическим исследованием. Атрофические процессы в эндометрии можно лечить лекарственными препаратами. Простая гиперплазия тоже требует медикаментозного лечения, но с учетом высоких рисков у постменопаузальных женщин — под контролем регулярных биопсий эндометрия.
Рак эндометрия обычно лечат хирургически — полностью удаляют матку (вместе с шейкой!), маточные трубы, яичники и близлежащие лимфатические узлы. Дальнейшая тактика зависит от того, насколько все запущено. Если заболевание распознали на ранней стадии, никакое лечение больше не требуется. В других случаях проводят лучевую терапию, гормонотерапию или химиотерапию.
Любые кровянистые выделения в постменопаузе — повод для обращения к врачу и проведения лечебно-диагностических процедур. Не надо ждать, что «само пройдет». Даже если кровотечение рано или поздно пройдет, нераспознанное заболевание за это время может зайти слишком далеко.
Атрофический вагинит — болезнь женщин “за 50», которая лечится интимом
» data-image-caption=»» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/01/vaginit.png?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/01/vaginit.png?fit=824%2C550&ssl=1″/>
Вагинальная атрофия (атрофический вагинит) — это истончение, высыхание и воспаление стенок влагалища из-за того, что в организме вырабатывается меньше женского гормона — эстрогена. Вагинальная атрофия возникает чаще всего после менопаузы.
| Прием гинеколога с высшей категорией | 1000 руб. |
| Консультативный прием врача по результатам анализов, по результатам УЗИ | 500 руб. |
| Расширенная кольпоскопия | 1500 руб. |
| Амино-тест на бактериальный вагиноз | 300 руб. |
| Медикаментозный аборт (все включено) | 4500 |
| Запись по телефону: 8-800-707-15-60 (бесплатный звонок) |
| *Клиника имеет лицензию на удаление новообразований |
Для многих женщин вагинальная атрофия не только делает половой акт болезненным, но также приводит к расстройству мочеиспускания. Из-за взаимосвязанной природы вагинальных и мочеполовых симптомов этого состояния, эксперты сходятся во мнении, что более точный термин для вагинальной атрофии и сопровождающих ее симптомов — «мочеполовой синдром менопаузы».
Простые, эффективные методы лечения мочеполового синдрома менопаузы — вагинальной атрофии и ее мочевых симптомов — доступны. Снижение уровня эстрогена приводит к изменениям в организме, но это не означает, что женщина должна жить с дискомфортом.
Симптомы вагинальной атрофии
При умеренном или тяжелом мочеполовом синдроме менопаузы наблюдаются следующие признаки и симптомы:
Когда обратиться к врачу
По некоторым оценкам, почти половина женщин в постменопаузе испытывает мочеполовой синдром менопаузы, хотя обращаются за лечением немногие. Женщины смиряются с симптомами или стесняются обсуждать их с гинекологом. А зря! Эта патология устраняется без хирургического вмешательства.
Запишитесь на прием к специалисту, если вы испытываете болезненные симптомы при половом акте, которые не разрешаются с помощью вагинального увлажнителя или смазки на водной основе. Также вам нужен гинеколог, если присутствуют вагинальные симптомы, такие как необычное кровотечение, выделения, жжение или болезненность.
Причины атрофического вагинита
Мочеполовой синдром менопаузы вызван снижением производства эстрогена. Уменьшение эстрогена делает влагалищные ткани более тонкими, сухими, менее эластичными и более хрупкими.
Упадок уровня эстрогена происходит:
Признаки и симптомы мочеполового синдрома менопаузы могут начать беспокоить в течение многих лет, предшествующих менопаузе, или могут не стать проблемой, пока не наступит менопауза.
Хотя это частое заболевание, не все женщины в период менопаузы испытывают мочеполовой синдром менопаузы. Некоторым помогают сохранить здоровые ткани влагалища регулярные сексуальные отношения с партнером.
Факторы риска
Определенные факторы могут способствовать возникновению мочеполового синдрома менопаузы. В этот круг входит:
Осложнения
Увеличивают риски развития следующих проблем со здоровьем:
Профилактика
Помогут предотвратить мочеполовой синдром менопаузы регулярные половые контакты с партнером. Сексуальная активность увеличивает приток крови к влагалищу, что помогает поддерживать здоровье тканей органа.
Диагностика
Диагностика атрофического вагинита может включать в себя:
Лечение
Для лечения мочеполового синдрома менопаузы с легкими симптомами гинеколог может сначала дать рекомендации:
Беспокоящие симптомы, которые не улучшаются при безрецептурном лечении лечатся следующими методами:
Актуальные эстрогены
Вагинальная эстрогенная терапия бывает в нескольких формах. Поскольку все они работают одинаково хорошо, лечащий врач может решить, какой из них лучше.
Системная терапия эстрогенами
Если сухость влагалища связана с другими симптомами менопаузы, такими как умеренные или сильные приливы, гинеколог предложить таблетки эстрогена, пластыри или гель, или эстрогенное кольцо с более высокой дозой.
Вместе с эстрогеном, если не удалена матка (гистерэктомия), назначается прогестин. Часто предпочтительным является оральный прогестерон, который химически идентичен гормону, который вырабатывает организм (биоидентичный). Также неплохо работают комбинации с эстроген-прогестиновыми пластырями.
Если отсутствует матка, можно использовать только эстроген. Поговорите с гинекологом, чтобы решить, является ли гормональное лечение подходящим, принимая во внимание любые медицинские проблемы и семейную историю болезни.
Другие методы лечения
Ученые работают над разработкой других методов лечения мочеполового синдрома менопаузы из-за опасений по поводу долгосрочного потенциала даже небольших доз эстрогена для увеличения риска рака молочной железы и эндометрии.
Если ранее был рак молочной железы
Если в анамнезе присутствует рак молочной железы, важно сообщить об этом лечащему врачу и рассмотреть следующие вопросы:
Образ жизни и домашние средства
Если женщина испытывает сухость или раздражение влагалища, она может почувствовать облегчение, если:
Альтернативная медицина
Некоторые альтернативные лекарства используются для лечения сухости и раздражения влагалища, связанных с менопаузой, но лишь немногие подходы подтверждаются данными клинических испытаний.
Интерес к комплементарной и альтернативной медицине растет, и ученые работают, чтобы определить преимущества и риски различных альтернативных методов лечения атрофического вагинита. Но прежде чем принимать какие-либо травяные или диетические добавки для симптомов перименопаузы или менопаузы, необходимо обязательно посоветоваться с гинекологом.
Вы должны понимать, что Управление по контролю за продуктами и лекарствами не регулирует продажу растительных добавок, и некоторые из них могут быть опасными или взаимодействовать с другими лекарствами, которые принимались ранее, подвергая риску здоровье.
Подготовка к встрече с гинекологом
Что нужно сделать, чтобы как следует подготовиться к консультации:
Вот некоторые основные вопросы, которые можно задать лечащему врачу:
Что можно ожидать от врача?
Лечащий врач задаст вопросы о ваших симптомах и сможет оценить гормональный статус. Вопросы, которые может задать врач, включают следующий перечень:
После беседы с гинекологом и сдачи анализов нужно строго выполнять все рекомендации врача, и тогда вагинальная атрофия обязательно отступит.
Вагинальная атрофия: этиологические аспекты и современные подходы к терапии
Вагинальная атрофия – симптом постменопаузы, характеризующийся эстрогендефицитным состоянием у женщин. Урогенитальный тракт особенно чувствителен к снижению уровня эстрогенов. 27–55% всех женщин в постменопаузе испытывают симптомы, связанные с урогенитальной атрофией (уга), затрагивающей половую функцию и качество жизни.
В клинической картине урогенитальных расстройств в климактерическом периоде выделяют симптомы, связанные с вагинальной атрофией, а также расстройства с мочеиспусканием (цистоуретральная атрофия). Если вазомоторные симптомы проходят со временем, признаки вагинальной атрофии прогрессируют. У 40–57% женщин отмечается сухость влагалища, жжение и зуд, диспареуния, кровотечения, недержание мочи, инфекции органов малого таза.
Стенки влагалища состоят из трех слоев: внутреннего, среднего мышечного и наружного соединительнотканного. Атрофические процессы захватывают мышечные и соединительнотканные структуры, а также мышцы тазового дна, уретры, мочевого пузыря. Особенно выражены они в слизистой влагалища, которая состоит из 4 основных слоев эпителиальных клеток: базального, парабазального (митотически активного), промежуточного гликогенсодержащего и поверхностного слущивающегося. Эстрогеновые рецепторы в основном располагаются в базальном и парабазальном слоях и практически отсутствуют в промежуточном и поверхностном. Дефицит эстрогенов блокирует митотическую активность базального и парабазального слоев эпителия, пролиферацию влагалищного эпителия. Следствием прекращения пролиферативных процессов являются исчезновение гликогена – питательной среды для лактобактерий, полное выведение лактобацилл, которые играют ключевую роль в предотвращении заболеваний урогенитального тракта. Вследствие расщепления гликогена при условии достаточного количества эстрогенов образуется молочная кислота, обеспечивающая кислую среду в пределах колебаний РН от 3,8 до 4,4. Подобный механизм приводит к подавлению роста патогенных и условно-патогенных бактерий. В период постменопаузы слизистая оболочка утрачивает защитные свойства, истончается, легко травмируется с последующим инфицированием.
Атрофия слизистой вульвы и влагалища характеризуется истончением, уменьшением вагинальной складчатости, побледнением, наличием петехиальных кровоизлияний, признаков воспаления, а также происходит потеря упругости тканей, подкожно-жировой клетчатки, выпадение лобковых волос, снижение секреторной активности бартолиниевых желез. Как правило, врачи диагностируют вагинальную атрофию на основании сочетания клинических симптомов, визуального осмотра и субъективных жалоб пациентки.
Для диагностики и оценки эффективности лечения вагинальной атрофии необходимо: РН и подсчет вагинального индекса созревания (ВИС, преобладание клеток базального и парабазального слоев), мультистероидный профиль крови.
ЭСТРОГЕНЫ
Эстрогены являются главными регуляторами физиологических процессов во влагалище. Все клинические рекомендации по лечению урогенитальной атрофии сходны в том, что наиболее эффективным методом лечения вагинальной атрофии является локальная гормональная терапия эстрогенами. Для лечения урогенитальной атрофии, сочетающейся с симптомами климактерия, используют системную гормональную терапию. Исследования показали, что локальная терапия устраняет симптомы вагинальной атрофии в 80–90% случаев, а системная терапия – в 75%. Ультранизкие дозы эстрогенсодержащих препаратов обладают выраженным кольпотропным эффектом. Учитывая слабое пролиферативное действие на эндометрий при использовании эстрогена, дополнительного введения прогестагена не требуется.
Роль дефицита эстрогенов у женщины в патогенезе урогенитальных расстройств в период менопаузы ни у кого не вызывает сомнений. Однако клиническая картина климактерического синдрома характеризуется широкой вариабельностью проявлений, поэтому не все урогенитальные расстройства в перименопаузе и постменопаузе могут быть объяснены недостаточным эффектом эстрогенов. С возрастом у женщин происходит значительное снижение уровня как эстрогенов, так и андрогенов. Так, уровень общего и свободного тестостерона, андростендиона и дегидроэпиандростерона в 45-летнем возрасте составляет в среднем 45%, в 60-летнем – около 30%, в 70-летнем – 10% от уровня этих гормонов у 20-летних женщин. Дефицит андрогенов, которому у женщин практически не уделяется внимания, оказывает негативное влияние на все органы и системы организма, особенно на половую систему. Применение ультранизких доз локальных эстрогенсодержащих препаратов является безопасным и эффективным подходом к предотвращению и лечению вагинальной атрофии, не имеет ограничений по возрасту и длительности применения.
АНДРОГЕНЫ
Андрогены у женщин, как и у мужчин, представлены дегидроэпиандростерона сульфатом (ДГЭА-С), дегидроэпиандростероном (ДГЭА), андростендионом, тестостероном и 5α дегидротестостероном (5-α-ДГТ). Однако в отличие от мужчин концентрация первых трех гормонов у женщин выше, чем концентрация двух последних. Секреция андрогенов в надпочечниках регулируется адренокортикотропным гормоном (АКТГ), в яичниках – лютеинезирующим гормоном (ЛГ). У женщин около 25% андрогенов образуется в яичниках, 25% – в надпочечниках, остальные синтезируются в периферических тканях. После наступления менопаузы основным местом синтеза андрогенов становятся яичники. Циркулирующий в крови тестостерон у женщин функционирует как прогормон, способный к конверсии в 5-α-ДГТ или 17-β-эстрадиол в тканях-мишенях.
Андрогеновые рецепторы широко представлены в головном мозге, в изобилии – в женской мочеполовой системе, хотя влияние андрогенов на состояние влагалища изучено недостаточно. Слизистая оболочка влагалища во время возбуждения выделяет муцин и вагинальный транссудат (эстрогензависимая функция), секреция которых у женщин является андрогензависимой. Известно также, что уровень эстрогенов в крови влияет на экспрессию андрогеновых рецепторов во влагалище: у женщин, получающих препараты эстрогенов, плотность андрогеновых рецепторов оказывается ниже, чем у тех, кто такие препараты не получает. При этом показано, что плотность андрогеновых рецепторов в менопаузе существенно уменьшается. Следовательно, уменьшение плотности андрогеновых рецепторов у женщин в постменопаузе в сочетании с возрастным снижением уровня андрогенов в сыворотке крови у них может быть причиной уменьшения андроген-чувствительности тканей влагалища.
Кроме того, в женской половой системе наряду с эстрогензависимыми эффектами регуляции регионарного кровообращения выявлена андрогензависимая NO-опосредованная вазодилатация. Таким образом, уровень эстрогенов у женщин является основным, но не единственным механизмом, обеспечивающим рост клеток гладкой мускулатуры влагалища, а также регулирующим метаболизм соединительной ткани и синтез оксида азота. При дефиците эстрогенов происходит истончение эпителия влагалища, что делает его восприимчивым к травмам и инфекциям. Однако вагинальный эпителий у женщин, которым вводили тестостерон или ингибиторы ароматазы, также демонстрировал увеличение числа слоев клеток, их толщины и числа митозов.
Андрогены усливают экспрессию NO-синтазы в проксимальном отделе влагалища, что проявляется в облегчении релаксации гладких мышц влагалища. Эстрогены, с другой стороны, снижают активность NO-синтазы и повышают активность L-аргиназы, что может привести к относительному дефициту оксида азота и ослаблению релаксации вагинальной ткани. Таким образом, можно предположить, что при нормальном уровне эстрогенов имеющаяся у женщины диспареуния может быть проявлением дефицита вазомиорелаксирующего влияния андрогенов на мочеполовую систему, мионейроваскулярной недостаточностью и спазмом мышц тазового дна на фоне дефицита андрогенов.
Возрастное снижение уровня андрогенов у женщин коррелирует с развитием симптоматики цистоуретральной и вагинальной атрофии. В мышцах тазового дна и нижних мочевых путях имеется огромное количество андрогеновых рецепторов, что делает эти группы мышц также высокочувствительными к анаболическим эффектам андрогенов у женщин. Несмотря на то, что эстрогензаместительная терапия оказывает выраженное положительное влияние на клинические проявления урогенитальных расстройств, у 30–40% системная заместительная гормональная терапия (ЗГТ) не эффективна, поэтому обычно назначают местную терапию эстриолом, основным биологическим эффектом которого является трофическое воздействие на нижние отделы урогенитального тракта. Однако даже при таком подходе у значительного числа пациенток проблемы сохраняются.
СОВРЕМЕННОЕ ВИДЕНИЕ
Зарубежные и российские исследования показывают, что применение тестостерона в постменопаузе может быть эффективным средством лечения вагинальной атрофии, никтурии, недержания мочи как на фоне системной и локальной ЗГТ, так и без нее. Необходим индивидуальный подход к лечению урогенитальных расстройств, учитывающий разные типы течения пери- и менопаузы. Так, пациентки с клинически и лабораторно (мультистероидный профиль, определяемый масс-спектральным методом) подтвержденным дефицитом андрогенов не должны получать препарат ЗГТ с антиандрогенными свойствами, в связи с тем что ряд жалоб, обусловленных дефицитом эстрогенов, могут только усугубиться. В то время как при сохраненной секреции андрогенов назначение препаратов с андрогенной активностью может привести к нежелательным явлениям андрогенизации: спровоцировать рост волос на лице, прибавку мышечной массы, повысить сальность кожи, чрезмерно повысить либидо. Поэтому при выборе препаратов для лечения урогенитальной атрофии учитываются индивидуальные особенности каждой конкретной пациентки, основываясь на показателях ее гормонального профиля.
Ряд экспериментальных исследований показали эффективность применения андрогенных препаратов –
ДГЭА и тестостерона у пациенток в постменопаузе с сексуальными нарушениями и урогенитальными расстройствами. Андрогенные препараты для лечения вагинальной атрофии применяются в качестве эффективных и безопасных средств в виде трансдермального геля тестостерона пропионата, перорального тестостерона ундеканоата интравагинального геля дегидроэпиандростерона (DHEA) – 0,25% (3,25 мг), 0,5% (6,5 мг) и 10% (13 мг). Крем с 0,5% DHEA оказался самым оптимальным для лечения вагинальной атрофии, он эффективен и существенно не влияет на сывороточный уровень эстрогенов.
Помимо перечисленных выше методов лечения вагинальной атрофии, на сегодняшний день существуют такие, как терапия препаратами эстриола с низкими и ультранизкими дозами (0,3 мг и менее 0,1 мг) в сочетании с лактобактериями, селективными модуляторами эстрогеновых рецепторов (оспемифен), а также терапия комбинацией конъюгированных эстрогенов и базедоксифена – селективного модулятора эстрогеновых рецепторов, известной как тканевой селективный эстрогенный комплекс (TSEC), эффективный в соотношении 20 мг/ 0,625 мг.
Таким образом, местная терапия имеет ряд преимуществ перед системным введением препаратов, позволяет избежать первичного метаболизма в лечении, максимально воздействует на эндометрий, имеет низкую гормональную нагрузку, минимальные побочные эффекты, не требует добавления прогестагенов, оказывает в основном локальный эффект. Учитывая патогенез вагинальной атрофии (дефицит не только эстрогенов, но и андрогенов, влияющих на качество мышечной ткани малого таза, сократительную способность мочевого пузыря) рекомендована также терапия с применением интравагинальных гелей (дегидроэпиандростерона), селективных тканевых эстрогеновых комплексов, селективных модуляторов эстрогеновых рецепторов и негормональных методов лечения, а также комбинированных препаратов, содержащих
ультранизкодозированный эстриол и лактобактерин.
Несмотря на то что эффективность лечения высока, не стоит забывать о профилактике заболевания: сохранение регулярной половой жизни очень важно в период менопаузы. При половом акте улучшается циркуляция крови, а семенная жидкость содержит половые стероиды, простагландины и незаменимые жирные кислоты, способствующие сохранению вагинальной ткани.