Дуральная торзия что это
В хирургии позвоночника повреждения твердой мозговой оболочки, как случайные, так и намеренные, встречаются не так уж и редко. При некоторых типах вмешательств, например, ревизионных ляминэктомиях, они встречаются чаще, при других, например, в условиях взрывных переломов или переломов дуг, они больше являются случайной находкой. Дуротомии являются обязательным этапом вмешательств по поводу интрадуральных образований или для разделения спаек спинного мозга.
Много усилий было потрачено на то, чтобы установить, с какой частотой встречаются повреждения твердой мозговой оболочки, однако единого мнения по этому вопросу до сих пор нет. В одном из обзоров, основанном на данных о хирургическом лечении 641 пациента, которым была выполнена декомпрессия на уровне поясничного отдела позвоночника, повреждения твердой мозговой оболочки во время операции отмечены у 88 (14%).2 В другом исследовании говорилось о частоте повреждений твердой мозговой оболочки в 5,3% при открытых дискэктомиях, 17,4% при ревизионных вмешательствах по поводу грыж межпозвонковых дисков, 7,6% при первичных вмешательствах на поясничном отделе позвоночника и 15,9% при аналогичных ревизионных вмешательствах.
Более высокая частота повреждений может быть связана с более обширными и ревизионными вмешательствами, при анкилозирующем спондилите, у пожилых пациентов. Риск осложнений при вмешательствах на позвоночнике, в т.ч. повреждений твердой мозговой оболочки, выше у пожилых пациентов.
Выявление во время операции повреждения твердой мозговой оболочки может повергнуть хирурга в замешательство, однако очень важно идентифицировать и эффективно ликвидировать это повреждение. К счастью, на сегодняшний день доступен целый ряд методик, позволяющих сделать это. В статьях на сайте мы остановимся на различных методах диагностики повреждений твердой мозговой оболочки, обсудим интраоперационные и послеоперационные методы их лечения.
а) Анатомия твердой мозговой оболочки. Твердая мозговая оболочка — это внешняя из трех оболочек, окружающих головной и спинной мозг, ограничивающая собой пространство, заполненное спинномозговой жидкостью (СМЖ). Латинский термин dura mater пословно означает «суровая мать», эта оболочка так названа благодаря свой «кожистой» структуре и потому, что она служит защитой для двух других мозговых оболочек — мягкой (pia mater) и паутинной (arachnoidea mater). Твердая мозговая оболочка (ТМО) в большей степени подвержена продольным разрывам, поскольку большинство составляющих ее волокон ориентированы в продольном направлении.
Дистально ТМО продолжается до уровня S2 позвонка, она заключает в себе паутинную оболочку и образует мешок, заполненный СМЖ (дуральный мешок). Внутри субарахноидального пространства располагается спинной мозг, заканчивающийся конусом спинного мозга на уровне L1-L2 позвонков. Пространство вокруг спинного мозга заполнено СМЖ, реабсорбция которой осуществляется в венозные сплетения через грануляции паутинной оболочки. Суточная продукция СМЖ составляет около 500 мл, таким образом объем ее полностью сменяется три раза в сутки. Из боковых желудочков головного мозга СМЖ попадает в третий и четвертый желудочки, оттуда в базальную цистерну и кортикальные и спинномозговые субарахноидальные пространства.
Повреждения твердой мозговой оболочки могут отличаться по размеру от мелкого недоступного невооруженному глазу дефекта до значительных разрывов, требующих восстановления или пластирования. Любые манипуляции в области ТМО сопряжены с риском ее повреждения. Например, разрыв может произойти при тупой или острой мобилизации мягких тканей или при удалении костных образований. Наиболее часто разрывы происходят при работе кусачками Керрисона, однако они также могут быть следствием сращения ТМО с резецируемыми костными элементами, послеоперационной перфорации острыми костными краями или на фоне эрозий ТМО при хроническом стенозе спинномозгового канала. Кроме того, перфорация ТМО происходит при различных медицинских вмешательствах, не связанных с операциями, например, при эпидуральном введении лекарственных препаратов или миелографии.
Часто повреждения ТМО поначалу не несут в себе какой-либо опасности для пациента, однако в отсутствие лечения они могут быть источником выраженного болевого синдрома или дискомфорта. Ранние симптомы нелеченых повреждений ТМО включают умеренную и выраженную позиционную головную боль, тошноту и рвоту, фотофобию и/или истечение СМЖ из операционной раны. Также разрывы ТМО сопряжены с повышенным риском развития глубокой инфекции. В отсутствии лечения или при пропуске повреждения ТМО возможно развитие отдаленных осложнений, которые могут привести к инвалидизации пациента. Круг осложнений включает, однако не ограничен такими состояниями, как функционирующий ликворный свищ, псевдоменингоцеле, повреждения корешков спинного мозга, арахноидиты с последующим хроническим болевым синдромом и, реже, менингит.
Также в литературе описаны такие осложнения, как внутричерепные кровоизлияния и базилярные грыжи головного мозга, являющиеся следствием изменения давления СМЖ.
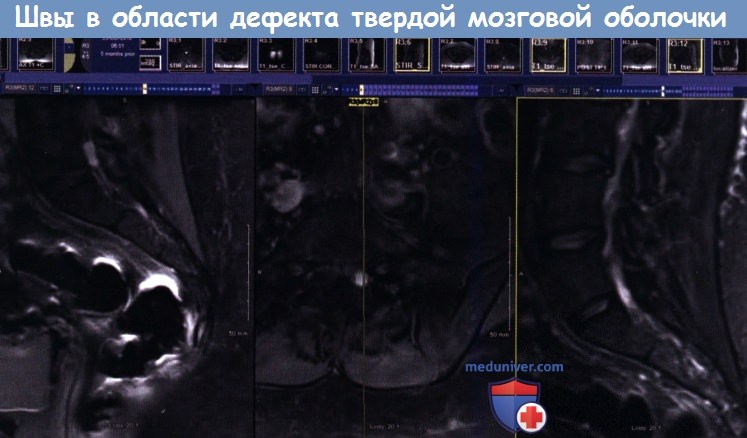
б) Клинический диагноз. Повреждение ТМО нередко выявляется во время операции как видимое глазом истечение СМЖ из зоны повреждения. Это может быть поток жидкости либо слабое поступление ликвора из точечного дефекта, смывающее кровь с поверхности ТМО. Постоянное поступление прозрачной жидкости по плевральному или субфасциальному дренажу также может быть следствием дуротомии. Коллапс дурального мешка или избыточное эпидуральное кровотечение также служат косвенными интраоперационными признаками повреждения ТМО. При обнаружении дефекта во время операции он должен быть немедленно устранен.
Если во время операции дефект дурального мешка обнаружен не был, в диагностике повреждения эффективны различные методы лучевого исследования. Магнитно-резонансная томография (МРТ), например, позволяет подтвердить диагноз псевдоменингоцеле, предполагающее наличие дефекта ТМО. Для обнаружения экстраарахноидальных скоплений жидкости используют Т2-взвешенные МР-томограммы. МРТ является предпочтительным методом диагностики, однако чередование жидкостных и плотных композитов на МР-томограммах позвоночника делает обнаружение дефекта ТМО достаточно затруднительным. МРТ также не позволяет напрямую визуализировать дефекты ТМО размером менее 1 см. Кроме того, после вмешательств на спинномозговом канале в зоне операции нередко присутствуют эпидуральные гематомы, которые бывает невозможно отличить от СМЖ.
В отличие от МРТ радионуклидная цистернография позволяет визуализировать даже небольшие дефекты ТМО, обнаружение изотопа за пределами субарахноидального пространства свидетельствует о наличии дефекта ТМО. Однако если на момент исследования активного истечения ликвора в области дефекта нет или если размер дефекта меньше разрешающей способности метода, выявить дефект невозможно. Кроме того, исследование сопряжено с введением в организм пациента радиоактивного изотопа, что также несет определенный риск.
Еще одной часто используемой методикой является КТ-миелография, которая позволяет выявить различные дефекты ТМО. Это достаточно чувствительная методика, которая кроме всего прочего позволяет оценить взаимоотношение выявленных экстрадуральных скоплений СМЖ с окружающими костными образованиями. Во многих случаях КТ-миелография является методом выбора при установке окончательного диагноза. Инвазивный характер исследования, однако, может привести к ирритации мягкой мозговой оболочки, а рентгеновское излучение несет в себе риск облучения пациента. Осложнения этой методики включают формирование нового дефекта ТМО в месте пункции и инфекционные осложнения.
Еще одним методом, позволяющим подтвердить наличие дефекта ТМО, является обнаружение β-2 трансферрина — белка, специфичного для СМЖ и перилимфы внутреннего уха, поэтому, если возникают сомнения относительно наличия дефекта, подходящим методом диагностики может быть электрофорез с иммунофиксацией белковых фракций. Исследование занимает три часа и требует всего 1-2 деконтаминированных капли жидкости. Чувствительность метода достигает 100%, специфичность — около 95%. Альтернативой β-2 трансферрину является (3-трейс протеин, концентрация которого в СМЖ также достаточно велика. Анализ на β-трейс протеин занимает около 20 минут. В исследовании 176 образцов показано, что чувствительность метода составляет 99%, а специфичность — 100%.
К сожалению, лаборатории многих клиник не обладают необходимыми для проведения этих исследований тест-системами, поэтому результаты в лучшем случае можно получить лишь спустя несколько дней.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Дуральная торзия что это
а) Терминология:
1. Синонимы:
• Эктазия твердой мозговой оболочки
2. Определения:
• Волнообразное расширение дурального мешка с вдавлением задних покровных пластинок тел позвонков
1. Общие характеристики дисплазии твердой мозговой оболочки:
• Наиболее значимый диагностический признак:
о Равномерное С-образное вдавление задних покровных пластинок тел позвонков и соответствующее расширение дурального мешка
• Локализация:
о Поясничный отдел > шейный, грудной отдел
• Размеры:
о Ограниченная → распространенная деформация
• Морфология:
о Расширенный дуральный мешок, ремоделирование стенок спинномозгового канала с характерным вдавлением задних покровных пластинок тел позвонков
2. Рентгенологические данные:
• Рентгенография:
о Равномерное ремоделирование задних покровных пластинок тел позвонков, расширение спинномозгового канала, + кифосколиоз
о Остеопения (гомоцистеинурия)
3. КТ признаки дисплазии твердой мозговой оболочки:
• КТ с КУ:
о Вдавление задних покровных пластинок тел позвонков → расширение спинномозгового канала:
— Лучше всего видно на сагиттальных срезах
о Истончение корней дуг, увеличение межпедикулярного интервала, эрозии передних и задних элементов позвонков, расширенный дуральный мешок, имеющий плотность, соответствующую СМЖ
• КТ-ангиография:
о ± расслоение или аневризмы артерий (если в основе патологии лежат синдромы Марфана или Элерса-Данло)
4. МРТ:
• Т1-ВИ:
о Вдавление задних покровных пластинок тел позвонков, расширение костных границ спинномозгового канала, расширение дурального мешка, ±кифосколиоз
о ± истончение корней дуг, латеральные менингоцеле
• Т2-ВИ:
о Аналогичные Т1-ВИ находки
о Более точно позволяет оценить расположение нервных образований относительно измененных элементов дурального мешка
• МР-ангиография:
о ± расслоение или аневризмы артерий (синдромы Марфана, Элерса-Данло)
5. Ультразвуковые данные:
• Монохромное УЗИ:
о Гипоэхогенные расширенные участки дурального мешка, расширение спинномозгового канала
6. Ангиография:
• Стандартная:
о Не используется для оценки характера деформаций позвоночника, применяется в первую очередь для диагностики сосудистых аномалий
о Аневризма восходящей аорты (конфигурация в виде «луковицы тюльпана») позволяет заподозрить синдром Марфана
7. Несосудистые рентгенологические исследования:
• Миелография
о Вдавление задних покровных пластинок тел позвонков, заполненный контрастом расширенный дуральный мешок, ±латеральные менингоцеле
8. Рекомендации по визуализации:
• МРТ также достаточно точно позволяет оценить особенности костной анатомии
• Кроме того, МРТ является наиболее эффективным методом диагностики кистозных изменений или опухолей спинного мозга, которые также могут быть причиной расширения спинномозгового канала
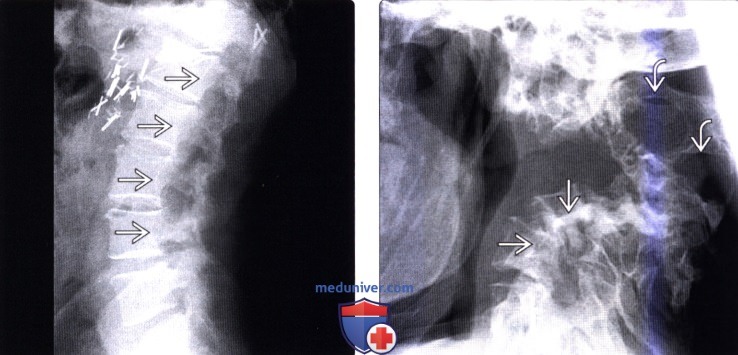
(Справа) На рентгенограмме в боковой проекции (НФ 1) определяются признаки ремоделирования задних покровных пластинок тел позвонков, тяжелая кифотическая деформация шейного отдела позвоночника и выраженное увеличение размеров межпозвонковых отверстий.
в) Дифференциальная диагностика дисплазии твердой мозговой оболочки:
1. Врожденная дисплазия позвоночника:
• Ахондроплазия
• Мукополисахаридоз
• Несовершенный остеогенез (поздняя форма)
• Обращайте внимание на семейный анамнез, клинические признаки соответствующих заболеваний
2. Опухоли и кистозные образования спинного мозга:
• Астроцитома
• Эпендимома
• Опухоль оболочек нерва
• Киста
• Правильный диагноз позволяют поставить соответствующие лучевые находки, характерные для этих заболевания
1. Общие характеристики дисплазии твердой мозговой оболочки:
• Этиология:
о Генетические заболевания:
— НФ1: первичное нарушение развития мезенхимального ростка
— Синдром Марфана: неизвестный первичный дефект соединительной ткани
— Синдром Элерса-Данло: > 10 различных типов дефектов синтеза коллагена
— Гомоцисгеинурия: недостаточность цистатионин-р-синтетазы
о Идиопатическая дисплазия
• Генетика:
о НФ1: аутосомно-доминантное заболевание (хромосома 17q12) о Синдром Марфана: аутосомно-доминантное заболевание
о Гомоцисгеинурия: аутосомно-рецессивное заболевание
о Синдром Элерса-Данло: аутосомно-доминантное заболевание
• Сочетанные аномалии:
о Латеральное грудное или поясничное менингоцеле, переднее крестцовое менингоцеле о Кифосколиоз
о Гипермобильность суставов, аномалии хрусталика, аневризмы и расслоение стенок артерий (дисплазия соединительной ткани)
о Новообразования центральной и периферической нервной системы (НФ1)
• Генетическая предрасположенность → первичная дисплазия твердой мозговой оболочки → снижение прочности мозговой оболочки → расширение дурального мешка, вторичное ремоделирование задних отделов тел позвонков и истончение корней дуг → дальнейшее увеличение размеров дурального мешка
2. Макроскопические и хирургические особенности:
• Расширенный и заполненный СМЖ дуральный мешок, ремоделированные задние отделы тел позвонков
• Твердая мозговая оболочка в зоне эктазии сильно истончается и становится хрупкой
3. Микроскопия:
• Истончение твердой мозговой оболочки на эктазированных участках
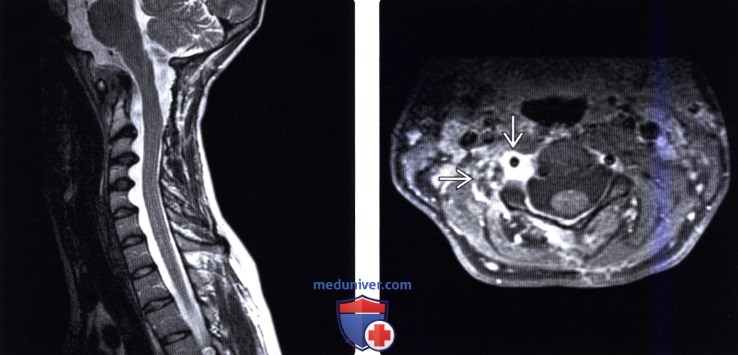
(Справа) FS Т1-ВИ с КУ подтверждает увеличение передне-заднего диаметра спинномозгового канала, а также наличие характерной для НФ 7 инфильтративной плексиформной нейрофибромы.
д) Клинические особенности:
1. Клиническая картина дисплазии твердой мозговой оболочки:
• Наиболее распространенные симптомы/признаки:
о Боль в спине → радикулопатия:
— Боль в спине от умеренной до выраженной имеет место более, чем у 50% пациентов с синдромом Марфана; выраженность дисплазии твердой мозговой оболочки коррелирует с тяжестью болевого синдрома
— Отмечается высокая частота дисплазии твердой мозговой оболочки (41%) у пациентов с синдромом Марфана, не характеризующегося болью в спине; таким образом, наличие дисплазии не обязательно означает наличие клинических проявлений
о Другие симптомы/признаки:
— Головная боль
— Недержание кала и мочи, тазовые нарушения
• Внешний вид пациента:
о НФ1: плексиформные нейрофибромы, кифосколиоз, глиомы зрительного нерва и астроцитомы другой локализации, кожные пятна цвета «кофе с молоком», пигментные пятна подмышечной области, ложные суставы костей конечностей
о Синдром Марфана: высокий рост, гипермобильность суставов, арахнодактилия, кифосколиоз, вывихи и подвывихи суставов, подвывих хрусталика
о Гомоцистеинурия: высокий рост, арахнодактилия, сколиоз, задержка психического развития, эпилепсия, подвывихи хрусталика
о Синдром Элерса-Данло: ± высокий рост, тонкая гиперэластичная кожа, гипермобильность суставов, хрупкость соединительной ткани
3. Течение заболевания и прогноз:
• Вариабельны и зависят от лежащей в основе заболевания патологии
• Заболеваемость и смертность связана в первую очередь с сосудистыми осложнениями:
о Хрупкость сосудов → предрасположенность к расслоению стенок и формированию аневризм артерий → преждевременная смерть
4. Лечение дисплазии твердой мозговой оболочки:
• Лечение направлено на компенсацию основного заболевания
• В более тяжелых случаях может быть показано закрытие менингоцеле, коррекция сколиотической деформации
е) Диагностическая памятка:
1. Следует учесть:
• К деформации задних покровных пластинок тел позвонков могут приводит три категории патологических процессов:
о Эктазия твердой мозговой оболочки
о Повышение внутриспинального давления
о Врожденная дисплазия позвоночника
• Для выработки адекватного плана лечения, проведения необходимого медико-генетического консультирования и определения прогноза необходимо точно установить лежащее в основе развития данной аномалии заболевания
2. Советы по интерпретации изображений:
• Точная диагностика основывается на выявлении характерных диагностических признаков заболевания и сопоставлении их с имеющимися клиническими данными
• Такими характерными признаками являются:
о Аневризма аорты в виде «луковицы тюльпана» → синдром Марфана
о Остеопороз → гомоцистеинурия о Ложные суставы костей, опухоли ЦНС/ПНС → НФ1
Редактор: Искандер Милевски. Дата публикации: 22.7.2019
Дуральная торзия. Второй мозг.
Дата добавления: 2015-08-31 ; просмотров: 7037 ; Нарушение авторских прав
Вы знаете, что спинной мозг покрыт тремя слоями ткани. Одна из них твердая мозговая оболочка, которая имеет склонность к скручиванию (торзии), возникающие при поворотах наклонах, это состояние дуральной торзии может зафиксироваться. Твердая мозговая оболочка не может расправиться, что приводит к дисфункции костного скелета на разных уровнях, начиная с краниального и заканчивая крестцом.
Если Вы прежде не исправите дуральную торзию, то те коррекции, которые Вы проводите при подобных нарушениях на механическом уровне, могут не дать стойкого результата.
По причине скручивания твердой оболочки спинного мозга у человека создается разная длина шага, например, правый шаг больше, чем левый шаг.
Именно поэтому люди, блуждая в лесу, не могут выйти на дорогу и ходят по кругу.
Я продемонстрирую Вам как это диагностировать и лечить. В начале покажу Вам традиционный способ диагностики, а потом короткий.
Методика коррекции: положение пациента лежа на животе, врач на вдохе пациента сближает крестец и затылочную кость друг к другу. Твердая мозговая оболочка расслабляется и торзия проходит. Таких манипуляций необходимо сделать 6-9.
Иногда работа с исправлением фиксаций восстанавливает состояние твердой оболочки спинного мозга.
Иногда, необходима коррекция работы правой и левой половины сердца, также как и правого и левого полушария головного мозга. Эта методика гармонизации предотвращает и агрегацию эритроцитов и удлиняет интервал PR на электрокардиограмме. Длина этого интервала характеризует длительность жизни, чем длиннее интервал PR, тем длиннее жизнь.
Эта методика называется «Второй мозг»!
Если этой методикой воздействовать на мозг, то результаты в некоторых случаях могут быть обратимыми. При воздействии на сердце результаты необратимы.
У пациента тестируют мышцу-индикатор, когда он производит счет. Если при этом мышца ослабевает, то это означает, что левое полушарие мозга и левая половина сердца функционируют не очень хорошо.
Коррекция производится следующим образом: врач поколачивает левую половину сердца одновременно со стороны спины и спереди двумя руками, в то время когда пациент напевает. Если мышца ослабевает на мелодию, которую напевает пациент, нужно откоррегировать правую половину сердца, нужно постукивать по правой половине сердца, но при этом пациент должен считать вслух. Постукивание производится одновременно спереди и сзади грудной клетки синхронно.
Коррекция головного мозга осуществляется так же, разница лишь в том, что постукивание делается по правой или левой височной кости, в зависимости от проблемы в той или другой половине мозга.
Коррекция сердца более надежней, чем коррекция мозга. Если проблема мозга не приоритетна: если пациенту врач кардиолог назначил препараты, не отменяйте их. Есть общее правило назначение препаратов, может отменять только тот, кто их назначил. Данную методику можно проводить при наличии кардиостимуляторов и симптомах аритмии.
Очень часто проблемы с полушариями мозга у пациентов не являются первоочередными. Проблемы сердца можно визуально обнаружить на вертикальной линии, на мочке уха. Эта линия не всегда прямо указывает на проблему в сердце. Но если есть даже функциональные нарушения эта бороздка на мочках ушей обязательно будет.
Методики коррекции «Второго сердца» желательно проводить каждому пациенту.
Тесты на токсичность и аллергичность с движением глаз.
Старение организма сопровождается накоплением свободных радикалов SOR+SOD=Н2О2+Н2О супероксидный радикал взаимодействует с супероксид-дисмутазой (ферментом) и получается перекись водорода и вода. Перекись водорода должна быть нейтрализована каталазой (фермент).
Если мышца-индикатор не слабеет, значит энергия в теле гармонизирована.
Тесты на аллергичность с движением глаз.
2. Выявление скрытых аллергий проводится одномоментной локализацией аллергена + терапевтической локализацией на точку аллергии.
Второй способ: на аллерген, находящийся на теле кладется южный полюс магнита + терапевтическая локализация точки аллергии.
3. Движение глаз в одном из 6 направлений устраняет полученную мышечную слабость, в результате реакции на аллерген.
Коррекция: аллерген помещается на язык или под южный полюс магнита, а врач проводит пассивное смещение глазных яблок(при закрытых глазах). в направлении провокации, усиливающей мышцу
Последним способом можно выявить все скрытые аллергии.
В норме на сахар мышцы ослабевают, но если немного подождать во времени и не убирать сахара с тела, то мышца усиливается. Так может происходить с любым плохим для организма веществом. Например: табак.
Если плохое вещество (пачку табака) носить в кармане весь день, то этот человек в конце дня будет чувствовать себя очень усталым, так как в течение дня для компенсации он тратил много энергии из всех источников
Провокация потирание кожи над зоной органа-
Дуральная артериовенозная фистула — редкая причина пульсирующего шума в ухе
Полный текст
Аннотация
В статье описаны клинические проявления дуральной артериовенозной фистулы, которая представляет собой аномальное сообщение между артериями твердой мозговой оболочки и венозными синусами или кортикальными венами. Информация об этиологии и патогенезе подобной мальформации в отечественной литературе ограничена немногочисленными публикациями. Диагностика основана на выявлении у больного визуальных (пульсация мочки уха) и акустических феноменов, а также шунта между задней заушной артерией (ветвью наружной сонной артерии) и венозными синусами мозга при нейровизуализации, в частности при магнитно-резонансной ангиографии. Оптимальной методикой лечения является нейрохирургическое вмешательство с использованием эндоваскулярной технологии.
Ключевые слова
Полный текст
АКТУАЛЬНОСТЬ
Шум в ухе или обоих ушах (тиннитус, от лат. tinnire — звенеть) представляет собой звуковое ощущение, не связанное с внешним акустическим стимулом [1]. Пациенты описывают его как звук, исходящий из одного или обоих ушей, находящийся внутри головы, или как внешний отдаленный шум, который «гудит, звенит, шипит, пульсирует» или имитирует другие знакомые звуки. Шум возникает периодически или ощущается постоянно, но неизменно снижает качество жизни пациентов [2].
Субъективный шум ощущается только пациентом, объективный — воспринимается в том числе окружающими и может быть зарегистрирован врачом с помощью фонендоскопа или специального прибора для регистрации отоакустической эмиссии [3], поскольку имеет внутренний источник звука. Последним часто становится патологический кровоток в сосудах (часто каменистой части сонной артерии), находящихся в непосредственной близости к среднему уху, что вызывает у пациента ощущение пульсации, особенно если громкость звука превышает порог слуха в этом ухе [4]. Наиболее опасными причинами пульсирующего шума могут быть артериовенозные мальформации и артериовенозные соустья твердой мозговой оболочки — дуральные фистулы [5, 6].
ДУРАЛЬНЫЕ АРТЕРИОВЕНОЗНЫЕ ФИСТУЛЫ
Дуральная артериовенозная фистула (ДАВФ) — аномальное сообщение между артериями твердой мозговой оболочки и венозными синусами или кортикальными венами [1]. Среди супратенториальных и инфратенториальных сосудистых мальформаций они составляют 6 и 35% соответственно. До недавнего времени ДАВФ считались относительно редкой патологией, однако в связи с возросшей частотой применения методов нейровизуализации (компьютерная, магнитно-резонансная томография) в последние годы диагностируются в большем проценте случаев [1–7]. По данным P. Jabbour и соавт. [8], распространенность ДАВФ составляет 0,17 случаев на 100 тыс. населения.
Большинство артериовенозных фистул представляют собой солитарные образования, однако встречаются описания множественных ДАВФ [2–9]. Мальформации могут развиться в любом возрасте, в том числе и детском, но чаще становятся находкой у пациентов 50–60 лет [7–9]. Выделяют врожденные и приобретенные ДАВФ [7–11]. Врожденные встречаются значительно реже; как правило, развиваются в первом триместре беременности в результате персистирующего сообщения между будущими артериальными и венозными сегментами первичного сосудистого сплетения или недоразвития промежуточной капиллярной сети [7]. Негативное влияние на ангиогенез могут оказывать родовая травма, внутриутробные инфекции, венозный тромбоз [3–12].
Последний фактор имеет важное значение в формировании приобретенных дуральных фистул. В одном из исследований подобная коморбидность выявлена в 72% случаев [10]. Развитию тромбоза венозного синуса и кортикальных вен способствуют гормональные изменения, связанные с беременностью, родами или, напротив, с использованием оральных контрацептивов; прокоагулянтное состояние крови: дефицит протеинов С и S, антитромбина III, мутации в генах II, V факторов свертывания; травмы головы, внутричерепные хирургические вмешательства, компрессия и окклюзия венозного синуса опухолью (чаще всего менингиомой), отиты и синуситы [9–13].
Существуют две гипотезы формирования ДАВФ в условиях синус-тромбоза. Согласно первой, повышение венозного давления, связанное с тромбозом и обструкцией венозного оттока, приводит к открытию ранее существующих физиологических шунтов в твердой мозговой оболочке с постепенной гипертрофией стенки синуса и формированием ДАВФ [13]. Изменение интракраниального гомеостаза на фоне тромбоза лежит в основе второй гипотезы. Длительная церебральная венозная гипертензия становится причиной развития локальной хронической гипоперфузии головного мозга, маркерами которой являются низкое церебральное перфузионное давление и снижение регионарного мозгового кровотока. В этих условиях усиление экспрессии фактора-1α (Hypoxia-inducible factor 1-alpha, HIF-1α) и эндотелиального фактора роста сосудов (Vascular endothelial growth factor, VEGF) приводит к аберрантному ангиогенезу и образованию ДАВФ [14].
Классификация
Среди неврологов и нейрохирургов наибольшее признание получили классификации дуральных соустий (1995) по Borden и Cognard [9–11]. В обеих делается акцент на оценку ретроградного лептоменингеального и коркового венозного сброса, характеристики которых важны для выбора тактики ведения пациента с ДАВФ [10–15]. В 2015 г. Комитетом по стандартам и правилам Общества нейроэндоваскулярной хирургии (Standard and Guidelines Committee for the Society of Neurointenventional Surgery) была предложена упрощенная классификация (SNIS S&G Classification), согласно которой ДАВФ делят на тип 1 (неагрессивный, без кортикального венозного рефлюкса) и тип 2 (агрессивный, с кортикальным венозным рефлюксом). Каждый из них может быть бессимптомным и симптомным, требующим срочного хирургического вмешательства [16].
Клиническая картина
При наличии ДАВФ больные чаще всего предъявляют жалобы на пульсирующий шум в ухе (81% случаев) и головную боль (15%), связанную с раздражением рецепторов менингеальных сосудов [9]. Внезапное появление головной боли и общемозговых симптомов — признак внутричерепного кровоизлияния (10%) [10].
Особенности других симптомов, возникающих в дебюте и при прогрессировании заболевания, во многом определяются локализацией фистул. Нарушение венозного оттока из глазных вен при каротидно-кавернозном соустье, локализованном в передней черепной ямке, может приводить к внутриглазной гипертензии, периокулярному отеку. Следствием этого являются развитие ретроорбитальной боли, периорбитального отека, хемоза, птоза, диплопии (вследствие наружной офтальмоплегии), а также снижение остроты зрения [7, 13], в редких случаях — ретинопатия и глаукома [9].
Пульсирующий шум в ухе может быть единственным симптомом фистулы поперечного или сигмовидного синусов, которые составляют до 80% при ДАВФ средней черепной ямки. Шум часто невыносимый, выматывающий больного. Возникновение его связано с увеличением объема крови, поступающей напрямую под высоким давлением из питающих артерий в венозные синусы, что вызывает в них турбулентный кровоток, синхронизированный с систолической фазой сердцебиения [13, 15]. В 40% случаев он выслушивается врачом при аускультации [17]. Затылочная артерия, участвующая в кровоснабжении ДАВФ этой области, обычно гипертрофирована. Ее прижатие к сосцевидному отростку уменьшает шум при физикальном осмотре [15]. Наличие пульсирующего шума в ухе, слышимого пациентом и/или врачом при аускультации над сосцевидным отростком, служит показанием к нейровизуализационному исследованию [10].
ДАВФ, расположенные субтенториально, — значимый фактор риска развития инфаркта ствола мозга, шейной миелопатии [10]. Изолированное поражение черепных нервов обусловлено их компрессией гипертрофированными питающими артериями или дренирующими венами [13].
Разрыв кортикальных вен, в зависимости от их расположения, приводит к внутримозговому, субарахноидальному или субдуральному кровоизлиянию. Кроме того, мощный шунтирующий поток, независимо от наличия или отсутствия тромбоза венозного синуса, может вызывать дистально от места поражения локальную или системную венозную гипертензию, развитие венозного геморрагического инфаркта. При повышении венозного давления возрастает и внутричерепное, вследствие этого в фазу декомпенсации клинические проявления заболевания могут напоминать таковые при объемном образовании (симптомы псевдоопухоли), начиная от головной боли, тошноты/рвоты, снижения остроты зрения вследствие отека соска зрительного нерва, до фокальных неврологических нарушений, включая гемигиперестезию, гемипарез, афазию. В тяжелых случаях развиваются когнитивная дисфункция, локальные или генерализованные судороги, сопор, кома [7, 9, 11].
Некоторые мальформации остаются бессимптомными или сохраняют стабильную клиническую и ангиографическую картину на протяжении многих лет, подвергаются спонтанной инволюции со стабилизацией или уменьшением неврологических симптомов. Факторы, предрасполагающие к регрессу заболевания, остаются неизвестными [8].
Диагностика
На начальном этапе для диагностики сосудистых мальформаций целесообразно проведение магнитно-резонансной (МР) ангио- и веносинусографии. Времяпролетная МР-ангиография (Time of flight, TOF) позволяет выявить особенности перестройки сосудистой системы при ДАВФ: увеличение числа и размера питающих артерий, расширение дренирующих вен, наличие сосудистой сети в дуральном синусе или мозговых оболочках, состояние коллатерального кровообращения и венозного оттока. МР-изображения, взвешенные по магнитной восприимчивости (susceptibility weighted imaging, SWI), обнаруживают признаки гипертензии кортикальных вен или небольшое кровоизлияние [15, 18–20].
Бесконтрастная компьютерная томография (КТ) головного мозга эффективна только в диагностике неблагоприятных исходов ДАВФ — кровоизлияний и отека мозга, однако КТ-ангиография способна идентифицировать измененные артерии и вены, выраженную сосудистую сеть в дуральном синусе или мозговых оболочках, тромбоз венозного синуса. В ряде случаев аномальная перестройка сосудистой сети может быть скрыта артефактами, исходящими от костей черепа. Используя алгоритмы реконструкции для удаления костных структур на изображениях, недостатки исследования могут быть устранены [12, 21]. Однако «золотым стандартом» диагностики ДАВФ остается цифровая субтракционная ангиография [2, 10]. Благодаря высокому пространственному и временному разрешению катетерная ангиография позволяет получить информацию о расположении и анатомических особенностях соустья, идентифицировать важные особенности ДАВФ, такие как наличие кортикального рефлюкса, обструкции венозного оттока, аневризмы [9, 15, 19].
Ультразвуковые методы, в частности дуплексное сканирование брахиоцефальных сосудов, транскраниальная допплерография и транскраниальное дуплексное сканирование интракраниальных сосудов, являются дополнительными методами диагностики ДАВФ, особенно для лиц с неспецифическими проявлениями. Основными преимуществами ультразвуковых методов являются неинвазивность, широкая распространенность и относительно невысокая стоимость по сравнению с остальными ангиовизуализационными методами диагностики [22]. У пациентов с ДАВФ при проведении ультразвуковых методов регистрируются более низкие индексы периферического сопротивления (индексы Гослинга и Пурсело) в питающих артериях, включая наружную сонную артерию и ее ветви (например, в затылочной артерии). Доказано, что значение индексов периферического сопротивления в питающих артериях коррелирует с эффективностью лечения и клинической эволюцией ДАВФ. Кроме того, у больных с ДАВФ транскраниальные методы выявляют высокую скорость кровотока, обратное направление потока крови и аномальную форму допплеровской волны (артериализация кровотока) в церебральных венах и синусах, глазных венах [23].
Независимо от исходных диагностических результатов или вариантов лечения, долгосрочное ангиографическое и/или ультразвуковое наблюдение рекомендовано всем пациентам с ДАВФ [24].
Лечение
Оптимальный метод лечения ДАВФ — полная элиминация фистулы. Эндоваскулярные вмешательства в виде трансартериальной, трансвенозной или комбинированной эмболизации в последние годы являются наиболее предпочтительными. В технически сложных случаях возможно проведение эндоваскулярного вмешательства с последующей микрохирургической резекцией [25]. При неэффективности или невозможности использования эндоваскулярных подходов осуществляют интраоперационную эмболизацию менингеальных артерий или вен, резекцию твердой мозговой оболочки [6]. Стереотаксическая радиохирургия применяется при высоком риске оперативного вмешательства или в случаях, когда проведение трансвенозной или трансартериальной эмболизации фистулы невозможно [12, 25]. С помощью гамма-ножа, линейных ускорителей или протонных пучков устранение фистулы достигается благодаря направленной доставке определенной дозы интенсивного излучения в зону ее локализации [26].
Ниже представлено клиническое наблюдение пациента, причиной пульсирующего шума у которого стала дуральная артериовенозная фистула.
КЛИНИЧЕСКИЙ ПРИМЕР
О пациенте
Пациент Д., 64 года, обратился с жалобами на постоянный пульсирующий шум за левым ухом, который усиливался в тишине, преимущественно в ночное время, в связи с чем Д. стал испытывать трудности засыпания.
Из анамнеза заболевания известно, что на протяжении последних двух лет Д. отмечал умеренное снижение слуха на оба уха, наблюдался у оториноларинголога с диагнозом нейросенсорной тугоухости. Периодически отмечал пульсирующий шум в левом ухе, который слышал во время засыпания, однако смена позы или поворот головы помогали устранить его. С сентября 2019 г. пульсация стала беспокоить независимо от времени суток с усилением в период отсутствия окружающего шума (ранние утренние часы, тихое помещение, шумоподавление и пр.). Нарушился ночной сон — не мог долго уснуть, смена положения тела и головы не давала должного эффекта. Стал тревожным, раздражительным из-за депривации сна и навязчивых ощущений. Лечился в неврологическом стационаре по направлению поликлиники, проводился курс сосудистой, нейрометаболической терапии без эффекта. Обращался в психоневрологический диспансер, где был установлен диагноз «Сенестопатическое расстройство». Назначены противотревожные, снотворные препараты.
Из анамнеза жизни известно, что в течение многих лет Д. страдает пароксизмальной формой мерцательной аритмии, артериальной гипертонией I степени; постоянно принимает антикоагулянты, гипотензивную терапию. Заболевания органов слуха, травмы, оперативные вмешательства области головы, перенесенные инфекционные заболевания отрицает.
Исследования при поступлении и окончательный диагноз
При осмотре пациента выявлена пульсация мочки уха слева, при аускультации заушной области над сосцевидным отростком выслушивался интенсивный пульсирующий шум, совпадающий с тонами сердца. Сопоставление анамнеза и клинических данных позволило заподозрить наличие сосудистой мальформации, требующей подтверждения с помощью ультразвуковых и/или нейровизуализационных методов исследования.
Проведенное дуплексное сканирование сосудов головы обнаружило признаки артериовенозной мальформации в бассейне левой наружной сонной артерии с артериализацией и усилением кровотока по внутренней яремной вене. Усиление скорости кровотока по задней околоушной артерии позволило предположить ее в качестве «питающего» сосуда (рис. 1). Контрастная МР-ангиография подтвердила наличие артериовенозного соустья с вовлечением поперечного и частично сигмовидного синусов слева (рис. 2).
Рис. 1. Дуплексное сканирование сосудов шеи
Примечание. Кровоток по общей сонной артерии (А) и наружной сонной артерии (Б) справа с нормальными индексами периферического сопротивления (PI и RI). Физиологический трехфазный кровоток по правой внутренней яремной вене (В). Кровоток по общей сонной артерии (Г) и наружной сонной артерии (Д) слева со сниженными индексами периферического сопротивления. Артериализация кровотока по левой внутренней яремной вене (Е). Значительно повышенный кровоток с низкими индексами периферического сопротивления по задней околоушной артерии (ветви наружной сонной артерии) в области артериовенозной мальформации (Ж).
Рис. 2. МР-ангиография (3D TOF-ангиография)
Примечание. А — сброс крови из ветвей наружной сонной артерии в левый поперечный синус; Б — аксиальная MIP-реконструкция: визуализируются нормальные артерии Виллизиева круга; слева расширенные и извитые ветви наружной сонной артерии (алые стрелки), из которых происходит сброс крови в поперечный и сигмовидный синусы (желтые стрелки), извитость и расширение дуральных вен вследствие полнокровия (голубые стрелки).
Пациент консультирован нейрохирургом, запланировано эндоваскулярное лечение фистулы.
ЗАКЛЮЧЕНИЕ
Дуральные артериовенозные фистулы — редкая форма патологии. Знание и правильная оценка ее симптомов — необходимое условие для адекватной интерпретации клинических данных, выбора методов обследования больного, определения прогноза заболевания и тактики лечения.





