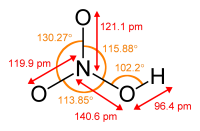
Азотная кислота ГОСТ 4461-77
наименование
Азотная кислота (HNO3) — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической решётками.
Азотная кислота смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы. Образует с водой азеотропную смесь с концентрацией 68,4 % и tкип120 °C при нормальном атмосферном давлении. Известны два твёрдых гидрата: моногидрат (HNO3·H2O) и тригидрат (HNO3·3H2O). Кислота ядовита.
Содержание
Физические и физико-химические свойства
Азот в азотной кислоте четырёхвалентен, степень окисления +5. Азотная кислота — бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C (при нормальном атмосферном давлении) с частичным разложением. Азотная кислота смешивается с водой во всех соотношениях. Водные растворы HNO3 с массовой долей 0,95-0,98 называют «дымящей азотной кислотой», с массовой долей 0,6-0,7 — концентрированной азотной кислотой. С водой образует азеотропную смесь (массовая доля 68,4 %, d20 = 1,41 г/см, Tкип = 120,7 °C)
При кристаллизации из водных растворов азотная кислота образует кристаллогидраты:
Твёрдая азотная кислота образует две кристаллические модификации:
Моногидрат образует кристаллы ромбической сингонии, пространственная группа P na2, a = 0,631 нм, b = 0,869 нм, c = 0,544, Z = 4;
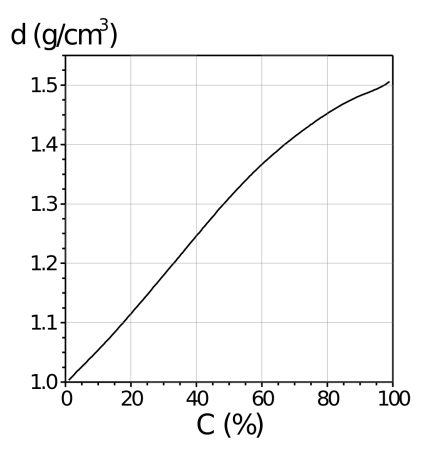
Плотность водных растворов азотной кислоты как функция её концентрации описывается уравнением
d(c) = 0,9952 + 0,564c + 0,3005c 2 − 0,359c 3
где d — плотность в г/см³, с — массовая доля кислоты. Данная формула плохо описывает поведение плотности при концентрации более 97 %.
Химические свойства
Высококонцентрированная HNO3 имеет обычно бурую окраску вследствие происходящего на свету процесса разложения:
При нагревании азотная кислота распадается по той же реакции. Азотную кислоту можно перегонять без разложения только при пониженном давлении (указанная температура кипения при атмосферном давлении найдена экстраполяцией).
Золото, некоторые металлы платиновой группы и тантал инертны к азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется её концентрацией.
HNO3 как сильная одноосновная кислота взаимодействует:
а) с основными и амфотерными оксидами:
в) вытесняет слабые кислоты из их солей:
При кипении или под действием света азотная кислота частично разлагается:
Азотная кислота в любой концентрации проявляет свойства кислоты-окислителя, при этом азот восстанавливается до степени окисления от +5 до −3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты. Как кислота-окислитель, HNO3 взаимодействует:
а) с металлами, стоящими в ряду напряжений правее водорода:
б) с металлами, стоящими в ряду напряжений левее водорода:
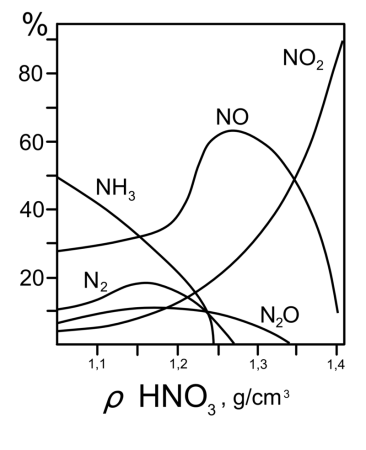
Все приведенные выше уравнения отражают только доминирующий ход реакции. Это означает, что в данных условиях продуктов данной реакции больше, чем продуктов других реакций, например, при взаимодействии цинка с азотной кислотой (массовая доля азотной кислоты в растворе 0,3) в продуктах будет содержаться больше всего NO, но также будут содержаться (только в меньших количествах) и NO2, N2O, N2 и NH4NO3.
Единственная общая закономерность при взаимодействии азотной кислоты с металлами: чем более разбавленная кислота и чем активнее металл, тем глубже восстанавливается азот:
С золотом и платиной азотная кислота, даже концентрированная, не взаимодействует. Железо, алюминий, хром холодной концентрированной азотной кислотой пассивируются. С разбавленной азотной кислотой железо взаимодействует, причем в зависимости от концентрации кислоты образуются не только различные продукты восстановления азота, но и различные продукты окисления железа:
Азотная кислота окисляет неметаллы, при этом азот обычно восстанавливается до NO или NO2:
и сложные вещества, например:
Некоторые органические соединения (например амины, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Некоторые металлы (железо, хром, алюминий, кобальт, никель, марганец, бериллий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
Смесь азотной и серной кислот носит название «меланж».
Азотная кислота широко используется для получения нитросоединений.
Смесь трех объёмов соляной кислоты и одного объёма азотной называется «царской водкой». Царская водка растворяет большинство металлов, в том числе золото и платину. Её сильные окислительные способности обусловлены образующимся атомарным хлором и хлоридом нитрозила:
3HCl + HNO3 ⟶ NOCl + 2[Cl]↑ + 2H2O
Au + HNO3 + 4HCl ⟶ H[AuCl4] + NO↑ + 2H2O
3Pt + 4HNO3 + 18HCl ⟶ 3H2[PtCl6] + 4NO↑ + 8H2O 
Нитраты
Азотная кислота является сильной кислотой. Её соли — нитраты — получают действием HNO3 на металлы и некоторые соединения неметаллов, оксиды, гидроксиды или карбонаты. Все нитраты хорошо растворимы в воде. Нитрат-ион в воде не гидролизуется.
Соли азотной кислоты при нагревании необратимо разлагаются, причём состав продуктов разложения определяется катионом:
а) нитраты металлов, стоящих в ряду напряжений левее магния (исключая литий):
б) нитраты металлов, расположенных в ряду напряжений между магнием и медью (а также литий):
в) нитраты металлов, расположенных в ряду напряжений правее ртути:
Нитраты в водных растворах практически не проявляют окислительных свойств, но при высокой температуре в твердом состоянии являются сильными окислителями, например, при сплавлении твердых веществ:
Цинк и алюминий в щелочном растворе восстанавливают нитраты до NH3:
С азотной кислотой не реагируют стекло, фторопласт-4.
Исторические сведения
Методика получения разбавленной азотной кислоты путём сухой перегонки селитры с квасцами и медным купоросом была, по видимому, впервые описана в трактатах Джабира (Гебера в латинизированных переводах) в VIII веке. Этот метод с теми или иными модификациями, наиболее существенной из которых была замена медного купороса железным, применялся в европейской и арабской алхимии вплоть до XVII века.
В XVII веке Глаубер предложил метод получения летучих кислот реакцией их солей с концентрированной серной кислотой, в том числе и азотной кислоты из калийной селитры, что позволило ввести в химическую практику концентрированную азотную кислоту и изучить её свойства. Метод Глаубера применялся до начала XX века, причём единственной существенной модификацией его оказалась замена калийной селитры на более дешёвую натриевую (чилийскую) селитру.
Во времена М. В. Ломоносова азотную кислоту называли крепкой водкой.
Промышленное производство, применение и действие на организм
Азотная кислота является одним из самых крупнотоннажных продуктов химической промышленности.
Производство азотной кислоты
Современный способ её производства основан на каталитическом окислении синтетического аммиака на платино-родиевых катализаторах (процесс Оствальда) до смеси оксидов азота (нитрозных газов), с дальнейшим поглощением их водой
Все три реакции — экзотермические, первая — необратимая, остальные — обратимые. Концентрация полученной таким методом азотной кислоты колеблется в зависимости от технологического оформления процесса от 45 до 58 %. Для получения концентрированной азотной кислоты либо смещают равновесие в третьей реакции путём повышения давления до 50 атмосфер, либо в разбавленную азотную кислоту добавляют серную кислоту и нагревают, при этом азотная кислота, в отличие от воды и серной кислоты, испаряется.
Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
Применение
Действие на организм
Юникод
В Юникоде есть алхимический символ азотной кислоты (лат. Aqua fortis ).
Снова природный индикатор
Ну как идет работа с индикаторами? Получается? Уже разобрались, как сделать индикатор кислотности самостоятельно? В прошлый раз я рассказала об этом достаточно подробно и даже показала, как это работает.
Теперь давайте поэкспериментируем еще с несколькими веществами.
Напоминаю, что с кислотами самодельный индикатор-каркаде дает ярко-оранжевую окраску. Так что, как определить кислоту в домашних условиях, вы знаете. А как индикатор из красного чая будет реагировать со щелочами?
Ну, теперь по порядку.
Приготовим немного раствора гидроксида натрия и прильем его к нашему самодельному индикатору:
Раствор становится темно-зеленым. Значит, в щелочной среде наш индикатор дает зеленую окраску. Кстати, многие индикаторы из растений дают именно зеленый цвет в щелочной среде (хотя, конечно, не все).
Теперь растворим в воде немного соды и прильем этот раствор к индикатору:
Точно также раствор стал темно-зеленым. Значит, пищевая сода имеет щелочную среду. Именно поэтому ее и используют для снижения кислотности желудка.
И стиральный порошок содержит вещества, имеющие щелочную реакцию. Именно они и обеспечивают удаление грязи с вещей:
А вот с железным купоросом не все так просто. При взаимодействии с индикатором он становится ярко-фиолетовым:
Или вот еще по-другому, чтобы было лучше видно:
Я уже писала про интересные свойства железного купороса при взаимодействии его с обычным черным чаем. А вот теперь вы знаете, что получается при взаимодействии его с красным чаем. Очень симпатичный фиолетовый цвет:
Ну и последний опыт на сегодня – взаимодействие красного чая с аммиаком:
Здесь никаких неожиданностей – нормальный темно-зеленый цвет. Да, аммиак – тоже щелочь.
Вот теперь вы сможете отличить кислоту от щелочи, если у вас будет самодельный индикатор. Не обязательно из красного чая, но пока ничего другого под рукой нет. А летом будет невообразимое множество самых разных природных индикаторов, на которых можно будет долго и с удовольствием тренироваться. Так что, подписывайтесь на обновления блога и не пропустите статьи об этих интересных веществах!
Да, кстати, есть среди вас автолюбители? Как вы относитесь к подушкам безопасности? Вы можете спросить, почему я задаю такой странный вопрос. А я отвечу, что подушки безопасности напрямую связаны с химическими реакциями. Как? Об этом вы можете прочитать вот здесь.
Ну а пока посмотрите на нашу весну:
Наталья Брянцева
Подписка на новости блога
Вы успешно подписаны на новости блога Kidschemistry.ru
К статье оставлено: 26 комментариев
Приглашаю вас принять участие в конкурсе на моем блоге) =)
Купил «Каркадэ-лепестки суданской розы. 100% каркадэ. Состав-лепестки суданской розы. Некалорийный продукт.» 2 чайные ложки залив кипятком — цвет чая ярко красный. кислоты сильные даже электролит не меняют его цвета разве что становится чище и выразительней. четко определился крот — четко зеленым. затем он потемнел а затем перешел в темно желтый цвет. Амиак тоже самое показал, на последней стадии как бы разделился раствор пополам-вверху темно желтый а в низу темновато зеленый. На соду питьевую — отреагировал черным цветом, пытался разглядеть под лампой-как бы темно зеленый оттенок но сомневаюсь. Пожалуйста, пишите что у кого получается. Очень интересно это та каркадэ что надо и есть ли другие разновидности?? попробую еще настоять сутки, охладить этот чаек и повторить опыт 8)
Наталья, снова большое спасибо! Мы пока мало что повторяли из ваших опытов, но уже собираем реактивы). Отыскалось немного чая красного, сейчас заварю, а вечером попробуем с детками поэкспериментировать).
Только покрепче чай заваривайте, а то мне в письмах некоторые пишут, что с ним не очень хорошо опыты получаются :- (
Отличный у вас блог)) Меня как химика-эколога прямо ностальгия пробирает)) С удовольствием читать буду
Анастасия, я очень рада общению с коллегами! Заходите почаще!
Очень интересные опыты. Я их только читаю, но все равно интересно.
Наталья, еще раз спасибо вам). Поэкспериментировали со всем, с чем пока смогли, заходите ко мне в гости, выложила большую статью о наших опытах.
Железо не может соединиться с водородом в процессе электролиза. Скорее всего, это идет разложение воды.
Насчет того, что электролит не поменял цвет с каркаде, я удивлена. Может электролит старый? Или это вовсе не электролит?
А с щелочью — все так и есть, должен быть насыщенный зеленый цвет, как у зеленки.
В каркаде присутствуют слабые органические красители, которые и меняют цвет в зависимости от среды.
Как приду в себя, обязательно напишу!
Наталья, поправляйтесь поскорее, крепкого вам здоровья!
Спасибо, Анна, будем поправляться!
Электролит, в целом, сложно испортить, но нужно учитывать, при какой температуре его хранили, вполне возможно, что разбавляли и т.д.
Красная капуста и Каркадэ чай : в 2 равные баночки (1-капуста спиртовой рр, 2 — каркадэ водный рр) равное количество индикатора. В каждую баночку отмерил шприцем равное количество электролита. третью баночку рядом для сравнения налил равное количество каркадэ. Отличие после реакции заметил между каркадэ и капустой. где каркадэ прозрачный раствор, а где капуста-понятно дело масляной немножко. но вот между каркадэ с электролитом и «оригиналом» каркадэ ооочень надо зрение напрягать чтобы увидеть отличие. после электролита немного светлее но мало заметно и неудобно. скажем раствор как был красный так и остался. Считаю, что если нету цветка как у Вас Наталья, то проверять чаем каркадэ кислоты-себя мучить. он годится только на щелочи. что касается такого вида каркадэ как Ваш цветок, то цвет вашего настоя очень похож на цвет настоя краснокачанной капусты, которая меняет выразительно цвета на кислоты- красным или его светлыми оттенками, а на щелочи зеленым и тд в зависимости от уровня рН. *CRAZY* Очень было бы интересно если еще заинтересовались любители химичить данной темой и повторили опыты обсуждаемой темы. может у кого есть другие варианты опытов и подходы к ним. был бы очень благодарен, а то я уже с чаем каркадэ как с индикатором дружить перестаю >:o
Виктор, чуть выше есть комментарий Анны, перейдите по ссылке и посмотрите на ее блоге статью «Открываем химическую лабораторию». Там она описывает, как делала опыты с чаем каркаде. Можете в комментариях к ее статье поинтересоваться, какой именно чай она использовала для опытов.
Наталья, спасибо Вам и скорейшего выздоровления! я здесь пытаюсь интриговать в опыты читателей. пусть собираются единомышленники =) насчет каркадэ терзает смутное сомнение а не кислыми ли консервантами законсервировали рассыпные цветочки каркадэ и кислотность уже достаточно большая в растворе получается. у меня с уксусом та же история. наверное с другими кислотами будет тоже самое. всякие приемы перепробовал- и кислоту приливал почуть чуть в настой и настой по чуть чуть капал в кислоту и тоже самое. чтото тут нечисто раз у людей другие цвета получаются. интригующе интересно всеже 8)
А про консервирование чая — думаю, тут вы правы. Я совсем забыла о консервантах. Просто уже лет десять такой чай не покупала. В качестве консерванта вполне может быть лимонная либо бензойная кислота. Хоть это и слабые кислоты, но свой вклад в общую реакцию среды запросто могут вносить.
Либо другой вариант — все-таки магазинный чай каркаде и раствор, сделанный из цветка — это разные вещи и сравнивать их не стоит. *UNKNOWN*
Полезное дело, например, можно кислотность почвы определять. Благодарю за интересную статью!
Ochen interesnii sait! nashla segodnia, 23 octiabria. Sama po obrazovaniu chimik. Postaraius provesti vashi opiti. Ogromnoe spasibo, Vam, Natalia.