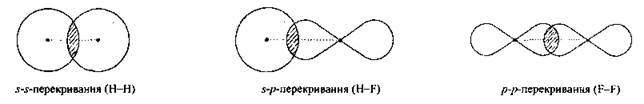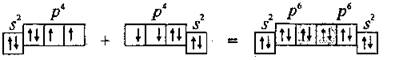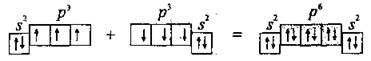Типы связей в молекулах органических веществ
Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Типы связей в молекулах органических веществ
Одна из характеристик химических связей — тип перекрывания орбиталей атомов в молекуле.
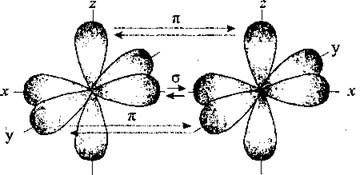
По характеру перекрывания различают σ-(сигма) и π‑(пи) связи.
| σ-Связь — это связь, в которой перекрывание орбиталей происходит вдоль оси, соединяющей ядра атомов. |
σ-Связь может быть образована любыми типами орбиталей (s, p, d, гибридизованными).
σ-Связь — это основная связь в молекуле, которая преимущественно образуется между атомами.
Между двумя атомами возможна только одна σ-связь.
 |  |
 |  |
 |  |
| π-Связь — это связь, в которой перекрывание орбиталей происходит в плоскости, перпендикулярной оси, соединяющей ядра атомов, сверху и снизу от оси связи. |
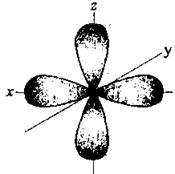
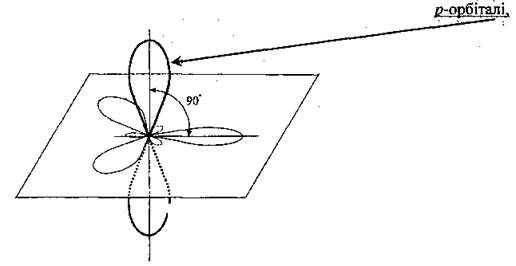
π-Связь образуется при перекрывании только р- (или d) орбиталей, перпендикулярных линии связи и параллельных друг другу.
π-Связь является дополнительной к σ-связи, она менее прочная и легче разрывается при химических реакциях.
С–С, С–Н, С–О
С=С, С=О
С≡С, С≡N
Таким образом, число сигма-связей ( σ-связей) в молекуле метана равно четырем:
В молекуле этилена число сигма-связей равно пяти, а также есть одна пи-связь (между атомами углерода):
В молекуле ацетилена всего три сигма-связи и две пи-связи:
H–C≡C–H
Добавить комментарий Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.
Метод определения пи и сигма связи
Новые аудиокурсы повышения квалификации для педагогов
Слушайте учебный материал в удобное для Вас время в любом месте
откроется в новом окне
Выдаем Удостоверение установленного образца:

«IQ и EQ как основа успешного обучения»
1. Если вещество нециклического строения: суммируем индексы в эмпирической формуле и отнимаем 1. Пример: H 3 PO 4 3+1+4=8-1=7
2. Если соединение нециклического строения, то 1 не отнимаем. Пример: C 6 H 6 6+6=12
3. Определение общего количества связей.
Валентность химических элементов умножаем на количество атомов, суммируем и делим на 2.
4. Определение π- связи.
От общего числа связи отнять количество σ – связи.
1.Определение σ – связи.
2. Определение общего количества связей.
3. Определение π- связи.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Химия: теория и методика преподавания в образовательной организации
Курс профессиональной переподготовки
Биология и химия: теория и методика преподавания в образовательной организации
Номер материала: ДБ-156652
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Всероссийская олимпиада школьников начнется 13 сентября
Время чтения: 2 минуты
Минпросвещения запустило конкурс «Директор года России»
Время чтения: 1 минута
В России каждый второй школьник хочет работать в IT
Время чтения: 1 минута
Учеба в школах в дни выборов в Госдуму будет идти в штатном режиме
Время чтения: 1 минута
В России запустят цифровые студенческие зачетки
Время чтения: 1 минута
Рособрнадзор дал рекомендации по проведению контрольных работ
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Сигма и пи связи
Ковалентные связи. Пи- и сигма- связи
Основные объекты биохимии.
Объектами изучения биоорганической химии являются белки и пептиды, нуклеиновые кислоты, углеводы, липиды, биополимеры, алкалоиды, терпеноиды, витамины, антибиотики, гормоны, токсины, а также синтетические регуляторы биологических процессов: лекарственные препараты, пестициды и др.
Изомерия органических соединений, ее виды. Характеристика видов изомерии, примеры.
Различают два вида изомерии: структурную и пространственную (т.е. стереоизомерию). Структурные изомеры отличаются друг от друга порядком связи атомов в молекуле, стереоизомеры — расположением атомов в пространстве при одинаковом порядке связей между ними.
Выделяют следующие разновидности структурной изомерии: изомерию углеродного скелета, изомерию положения, изомерию различных классов органических соединений (межклассовую изомерию).
Изомерия углеродного скелета обусловлена различным порядком связи между атомами углерода, образующими скелет молекулы. Например: молекулярной формуле С4Н10 соответствуют два углеводорода: н-бутан и изобутан. Для углеводорода С5Н12 возможны три изомера: пентан, изо-пентан и неопентан. С4Н10 соответствуют два углеводорода: н-бутан и изобутан. Для углеводорода С5Н12 возможны три изомера: пентан, изо-пентан и неопентан.
Изомерия положения обусловлена различным положением кратной связи, заместителя, функциональной группы при одинаковом углеродном скелете молекулы
Межклассовая изомерия- изомерия веществ, принадлежащих к разным классам органических соединений.
Современная классификация и номенклатура органических соединений.
В настоящее время широко используется систематическая номенклатура- IUPAC- международная единая химическая номенклатура. Правила ИЮПАК основываются на несколько систем:
1) радикально-функциональная ( в основе названия лежит название функц-й группы),
2) соединительная (названия составляют из нескольких равноправных частей),
3) заместительная (основой названия служит углеводородный фрагмент).
Ковалентные связи. Пи- и сигма- связи.
Ковалентная связь являетсся основным типом связи в органических соединениях.
Это связь, образованная перекрытием пары валентных электронных облаков.
Пи-связь- это ковалентная связь, образующаяся путем перекрывания р-атомных орбиталей.
Сигма-связь- это ковалентная связь, образующаяся при перекрывании s-атомных орбиталей.
Если между атомами в молекуле образуются как s-, так и р-связи, то образуется кратная (двойная или тройная) связь.
6. Современные представления о структуре органических соединений. Понятие «химическое строение», «конфигурация», «конформация», их определение. Роль структуры в проявлении биологической активности.
В 1861 году А.М. Бутлеровым была предложена теория химического строения органических соединений, лежащая в основе современных представлений о структуре орг. соединений,которая состоит из следующих основных положений:
1.В молекулах веществ существует строгая последовательность химического связывания атомов, которая называется химическим строением.
2.Химические свойства вещества определяются природой элементарных составных частей, их количеством и химическим строением.
3.Если у веществ с одинаковым составом и молекулярной массой различное строение, то возникает явление изомерии.
4.Так как в конкретных реакциях изменяются только некоторые части молекулы, то исследование строения продукта помогает определить строение исходной молекулы.
5.Химическая природа (реакционная способность) отдельных атомов в молекуле меняется в зависимости от окружения, т.е. от того, с какими атомами других элементов они соединены.
Понятие «химическое строение» включает представление об определенном порядке соединения атомов в молекуле и об их химическом взаимодействии, изменяющем свойства атомов.
Конфигурация — относительное пространственное расположение атомов или групп атомов в молекуле химического соединения.
Конформация — пространственное расположение атомов в молекуле определенной конфигурации, обусловленное поворотом вокруг одной или нескольких одинарных сигма-связей
Сигма связь-ковалентная связь образованная при перекрывании атомных s-электронных облаков, происходит вблизи прямой, соединяющей ядра взаимодействующих атомов (т.е. вблизи оси связи)
В образовании сигма-связи могут принимать участие p-электронные облака, ориентированные вдоль оси связи. в молекуле HF ковалентная сигма-связь возникает вследствие перекрывание 1s-электронного облака атома водорода и 2p-электронного облака атома фтора.
Химическая связь в молекуле F2 тоже сигма связь, она образована 2p-элект. облаками двух атомов фтора.
Пи-связь — ковалентная связь, при взаимодействии p-электронных облаков, ориентированных перпендикулярно оси связи, образуются не одна, а две области перекрывания, расположенные по обе стороны от этой связи.
Примеры:
в молекуле N2 атомы азота связаны в молекуле тремя ковалентными связями, но связи неравноценны одна из них сигма, две другие пи-связи.
вывод о неравноценности связей в молекуле подтверждается тем, что энергия их разрыва различна; пи-связь является непрочной
Общая химия
3. Химическая связь
3.5. Сигма — и пи-связь
Пространственно различают два типа связи — сигма — и пи-связь.
1. Сигма-связь (σ-связь) — простой (одинарный) ковалентная связь, образующаяся перекрыванием электронных облаков по линии, соединяющей атомы.
Связь характеризуется осевой симметрией:
В образовании σ-связи могут принимать участие как обычные, так и гібридизовані орбитали.
Пи-связь (π-связь). Если у атома после образования σ-связи остались неспаренные электроны, он может использовать их на образование второго типа связи, который называют π-связью. Рассмотрим его механизм на примере образования молекулы кислородаO2.
Два неспаренные р-электроны в атоме Кислорода могут образовать две совместные ковалентные пары с электронами второго атома Кислорода:
Одна пара идет на образование σ-связи:
Другая, перпендикулярная к ней, — на образование π-связи:
Еще однаp-орбиталь (рв), как иs-орбиталь, на которой находятся по две спаренные электроны, участия в связи не берут и не обобществляются.
Аналогичным образом при образовании органических соединений (алкенов и алкадієнів) послеsp2-гибридизации у каждого из двух атомов Углерода (между которыми образуется связь) остается по одной негібридизованій р-орбитали.
которые размещаются в плоскости, которая является перпендикулярной к оси соединения атомов Карбона:
В сумме σ — и π-связи дают двойную связь.
Тройная связь образуется аналогично и состоит из одной σ-связи (рх) и двух я-связей, которые образованы двумя взаимноперпендикулярными парамиp-орбиталей (ру,pz):
Пример: образование молекулы азотаN2.
Электронная формула атома Азота-7N 1s22s22p3или
В результате образования трех общих электронных парN≡Nкаждый атом Азота приобретает устойчивую электронную конфигурацию инертного элемента 2s22p6(октет электронов).
Тройная связь возникает и при образовании алкінів (в органической химии).
В результатеsг-гибридизации внешней электронной оболочки атома Углерода образуется двеsр-орбитали, расположенные по оси 0Х. Одна из них идет на формирование в-связи с другим атомом Углерода (вторая — на формирование σ-связи с атомом Водорода). А две не гібридизовані р-орбитали (ру,pz) размещаются перпендикулярно друг к другу и к оси соединения атомов (0Х).
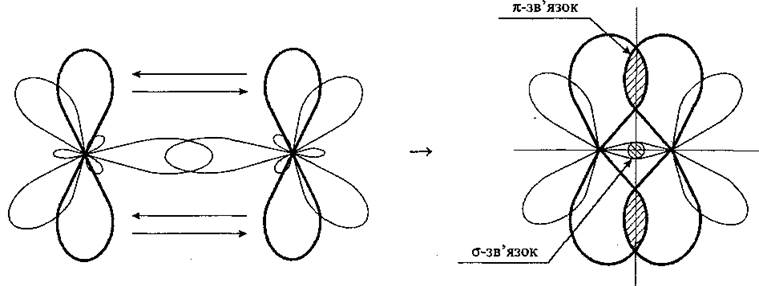
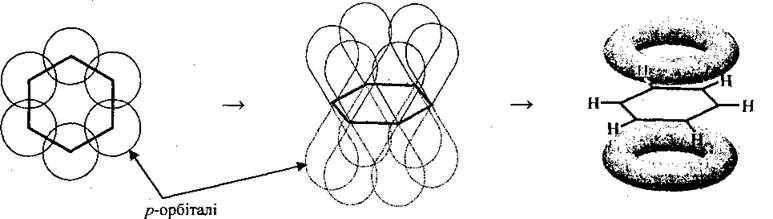
С помощью π-связи формируется молекула бензену и других аренов.
Длина связи (ароматического, «полуторного», сказывается
Все шесть атомов Углерода имеют общую π-электронное облако, плотность которой локализована над и под плоскостью ароматического ядра и равномерно распределена (делокалізована) между всеми атомами Углерода. По современным представлениям она имеет форму тороида:
Под длиной связи понимают расстояние между центрами ядер атомов Углерода, участвующих в связи.
π-Связи возникают между атомами, уже соединенными σ-связью (при этом образуются двойные и тройные ковалентные связи).
π-Связь слабее σ-связи из-за менее полного перекрывания р-АО.
Поэтому поляризуемость π-связи значительно выше, чем σ-связи.
Как узнать сигма или пи связь
РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
В образовании σ-связи могут принимать участие как обычные, так и гібридизовані орбитали.
Два неспаренные р-электроны в атоме Кислорода могут образовать две совместные ковалентные пары с электронами второго атома Кислорода:
Одна пара идет на образование σ-связи:
которые размещаются в плоскости, которая является перпендикулярной к оси соединения атомов Карбона:
В результате образования трех общих электронных пар N≡N каждый атом Азота приобретает устойчивую электронную конфигурацию инертного элемента 2 s 2 2 p 6 (октет электронов).
С помощью π-связи формируется молекула бензену и других аренов. Длина связи (ароматического, «полуторного», сказывается 
1 Под длиной связи понимают расстояние между центрами ядер атомов Углерода, участвующих в связи.
Связь Сигма и Пи 2021
Что такое облигация Сигма?
Молекулярные связи
Молекулы образуются, когда атомы обмениваются или обмениваются электронами посредством химической связи. Существуют, по существу, три типа облигаций. Ионные связи, металлические связи и ковалентные связи. В ионных связях атомы будут просто обмениваться электроном так, чтобы один атом стал заряженно заряженным, а другой отрицательно заряжен, заставляя их притягиваться электромагнитной силой. В металлических связях электроны будут равномерно распределены по всей молекуле, создавая море свободных, делокализованных электронов, обволакивающих положительно заряженные ионы, притягиваемые к электронам.
В ковалентных связях электроны разделены, и способ, которым они делятся, осуществляется через облака вероятности электронов и орбитали, в которых они расположены, перекрываясь грубо симметричным образом.
Орбитальные и сигма-облигации
Сигма-связи и сигма-орбитали
Электроны, составляющие сигма-связь, будут находиться внутри сигма-орбиталей и, следовательно, будут находиться где-то вдоль оси, соединяющей ядра связанных атомов. Однако сигма-связь может быть стабильной или неустойчивой в зависимости от того, находятся ли электроны в орбитальной сигма-связи или антисвязывающей орбите.
Сигма-связывающие орбитали будут находиться в промежутке между ядрами, тогда как антисвязывающие орбитали будут вдоль оси, соединяющей ядра, но с боков атомов, противоположных пространству между ними. Сигма-связь будет устойчивой, если большее количество электронов находится в связанных орбиталях и нестабильно, если больше в антисвязывающих орбиталях или если в обоих имеется одинаковое количество электронов.
Что такое связь Pi?
Связи Pi представляют собой связи между атомами внутри молекул, где электроны находятся выше и ниже оси, соединяющей ядра соединенных атомов, но не вдоль оси. Это второй тип связи, который образуется внутри молекулы после сигма-связи.
Pi и п орбитали
Причина, заключающаяся в том, что pi-связи образуются выше и ниже оси сцепления, но не вдоль нее, состоит в том, что они обычно образуются из перекрывающихся орбиталей, таких как п орбиталей на связанных атомах. Эти орбитали не имеют электронной плотности в ядре. В результате электроны, образующие связи pi, которые образуются из перекрывающихся п орбитали всегда будут кластеризоваться в области, которая непосредственно не примыкает к ядру. Связи Pi могут также образовываться между другими атомными орбиталями, такими как d орбиталей, которые имеют общие черты с п орбитали.
Pi-связи и pi-орбитали
когда п орбитали разных атомов перекрываются, они создают молекулярные pi-орбитали, которые позволяют образовывать pi-связи. Связь может снова быть стабильной или неустойчивой в зависимости от орбиты, в которой находится электрон. Связывание pi будет устойчивым, если больше электронов находится в орбиталях, связывающих пи. Он будет неустойчивым, если на анти-склеивающих орбиталях больше, или если одинаковое число в обоих.
Сходства между сигма-облигациями и pi-облигациями
Sigma-связи и pi-связи основаны на определенных молекулярных орбиталях, которые получены из перекрытия отдельных атомных орбиталей, например, s орбиталей в случае сигма-связей и п орбиталей в случае pi-связей. Они также могут быть стабильными или неустойчивыми в зависимости от того, находятся ли электроны в молекулярных орбиталях связи или антисвязывающих молекулярных орбиталях.
Различия между сигма-облигациями и пи-облигациями
Несмотря на их сходство, существуют важные различия.
Сигма-облигации против пи-облигаций
| Sigma bond | Связь Pi |
| Атомные орбитали перекрываются вдоль оси сцепления | Атомные орбитали перекрываются сверху и снизу оси сцепления |
| Первые связи образуют между атомами внутри молекул | Вторые связи образуют между атомами внутри молекул |
| Сформированные из перекрывающихся орбиталей, таких как s орбитали | Сформированные из перекрывающихся орбиталей, таких как п орбитали |
| Перекрывающиеся орбитали, перпендикулярные орбитам pi | Перекрывающиеся орбитали, перпендикулярные орбитам сигма |
Основная информация: Sigma and Pi Bonds
Сигма-связь представляет собой связь между атомами внутри молекулы, которая образуется s орбиталей, перекрывающихся вдоль оси, соединяющей соединенные ядра. Он формируется первым и его устойчивость зависит от того, как электроны распределены в сигма-склеивании и антисвязывающих орбиталях. Связи Pi представляют собой молекулярные связи, образующиеся часто от перекрытия п орбиталей от разных атомов. Электроны, составляющие pi-связи, будут распределены выше и ниже оси, соединяющей ядра связанных атомов, но не вдоль оси. Стабильность этих связей также зависит от связывания и антисвязывающих pi-орбиталей. Сигма-облигации будут первыми связями, образующимися в молекулах, тогда как pi-связи будут вторыми связями. Связи Pi также образуются из атомных орбиталей, ориентированных перпендикулярно тем, которые составляют сигма-связи.