Химические элементы
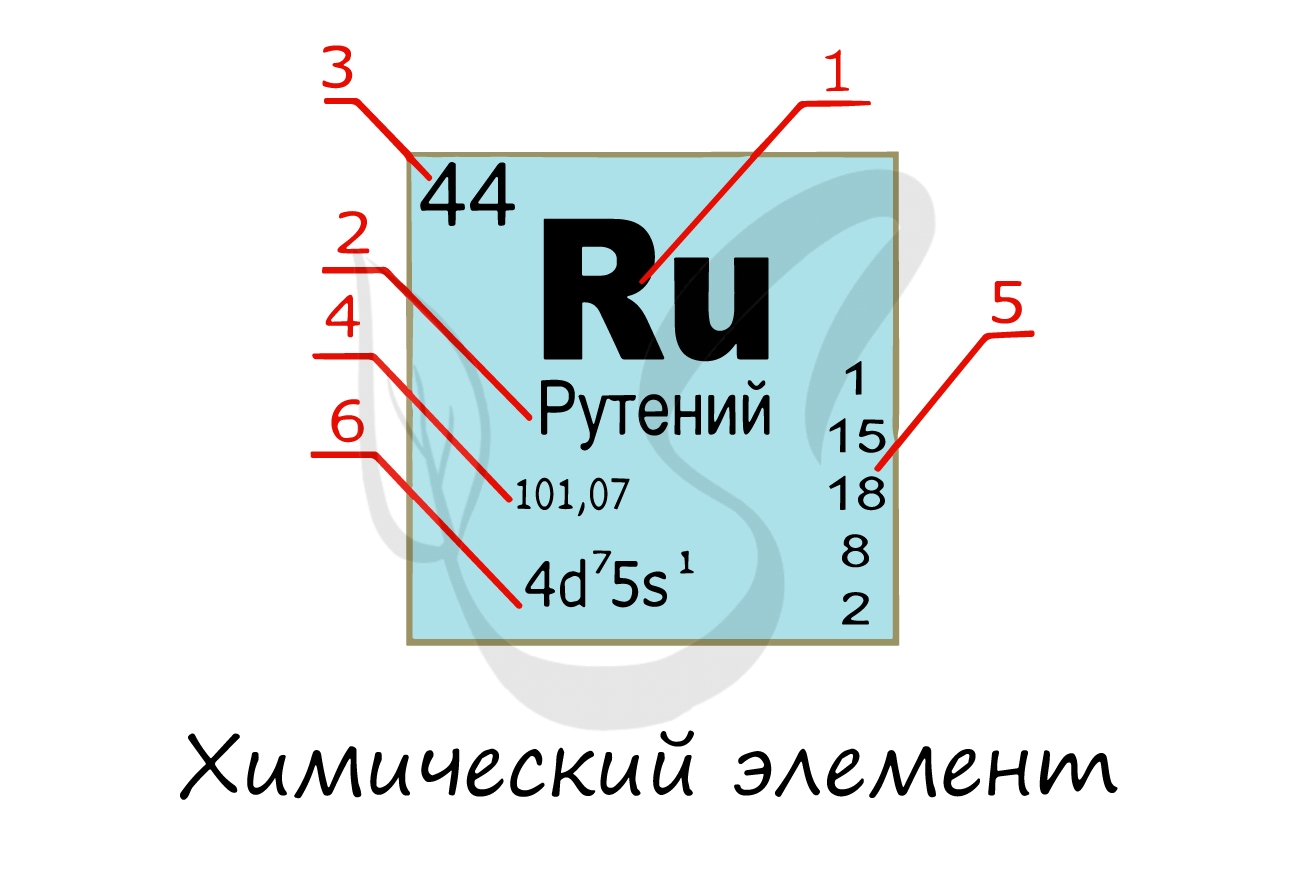
Химический элемент
Надо заметить, что на экзамене часто из карточки элемента скрывают распределение электронов и конфигурацию внешнего уровня. Тем не менее, если вы успешно освоили предыдущую тему, то для вас не составит труда написать электронную конфигурацию атома зная его порядковый номер в таблице Д.И. Менделеева (номер уж точно не тронут!))
Протоны, нейтроны и электроны
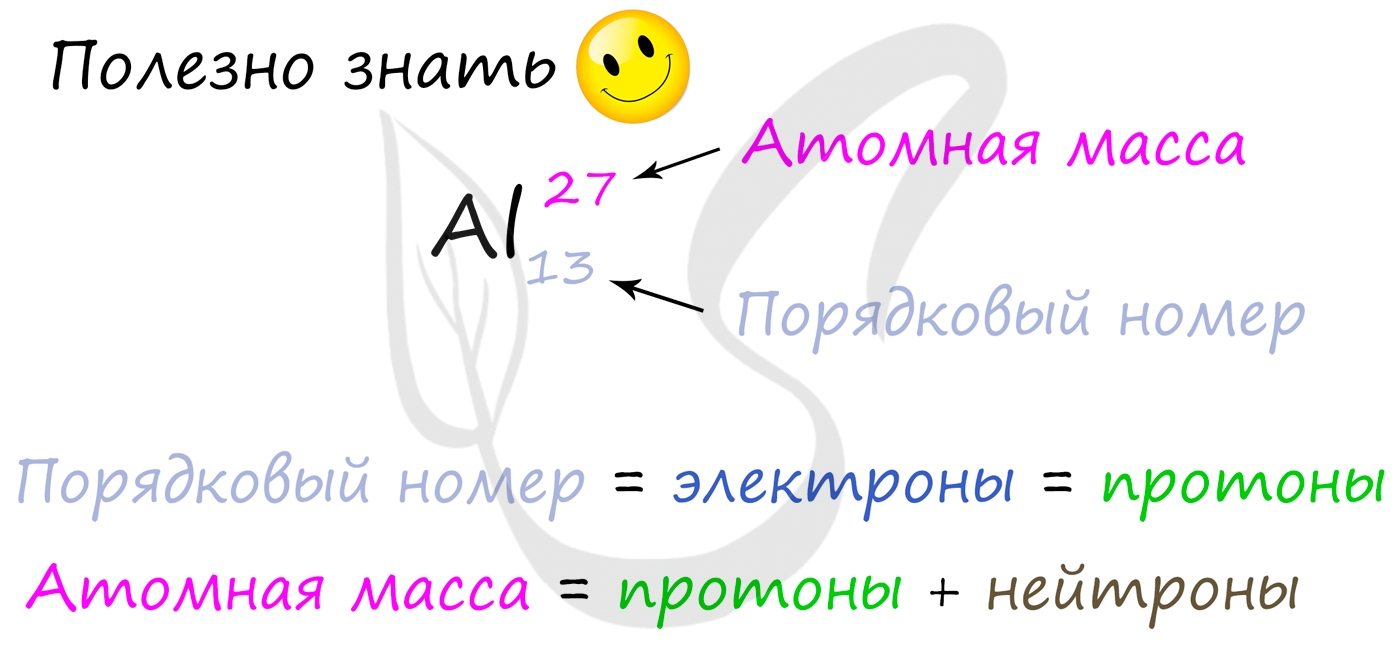
Вы уже знаете, что порядковый номер элемента в периодической таблице Д.И. Менделеева равен числу протонов, а число протонов равно числу электронов.
Для того чтобы найти число нейтронов в атоме алюминия, необходимо вычесть из атомной массы число протонов:
Получается, что в атоме алюминия 14 нейтронов. Посчитайте число нейтронов, электронов и протонов самостоятельно для атомов бериллия, кислорода, меди. Решение вы найдете ниже.
Если вы поняли суть и научились считать протоны, нейтроны и электроны, самое время приступать к следующей теме.
Изотопы
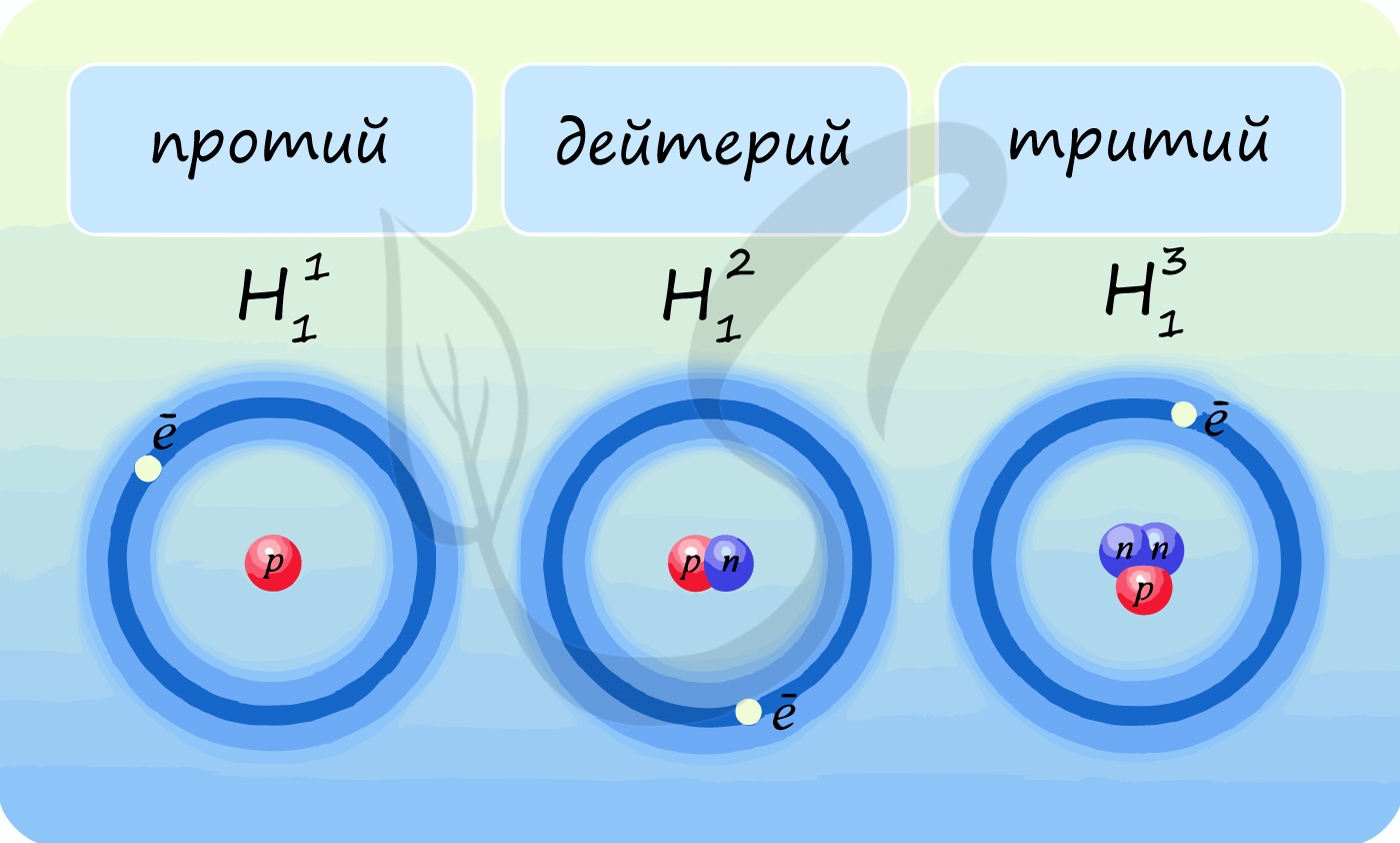
Лучше всего объяснить, что такое изотопы наглядным примером. Широко известны три изотопа водорода: протий, дейтерий и тритий.
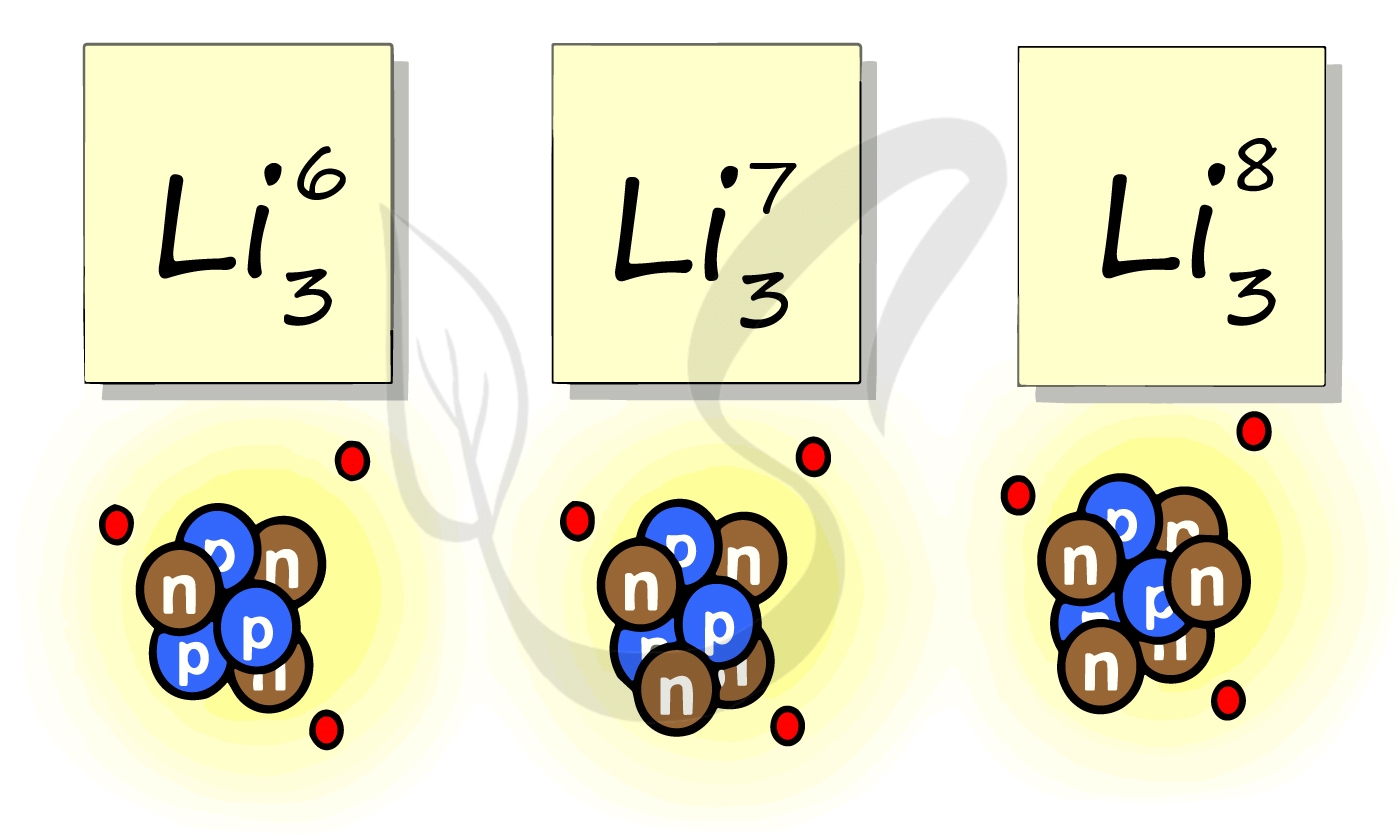
Рассмотрим пример с изотопами лития. Самостоятельно посчитайте количество нейтронов у каждого изотопа. Найдите тот, который включен в таблицу Д.И. Менделеева.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
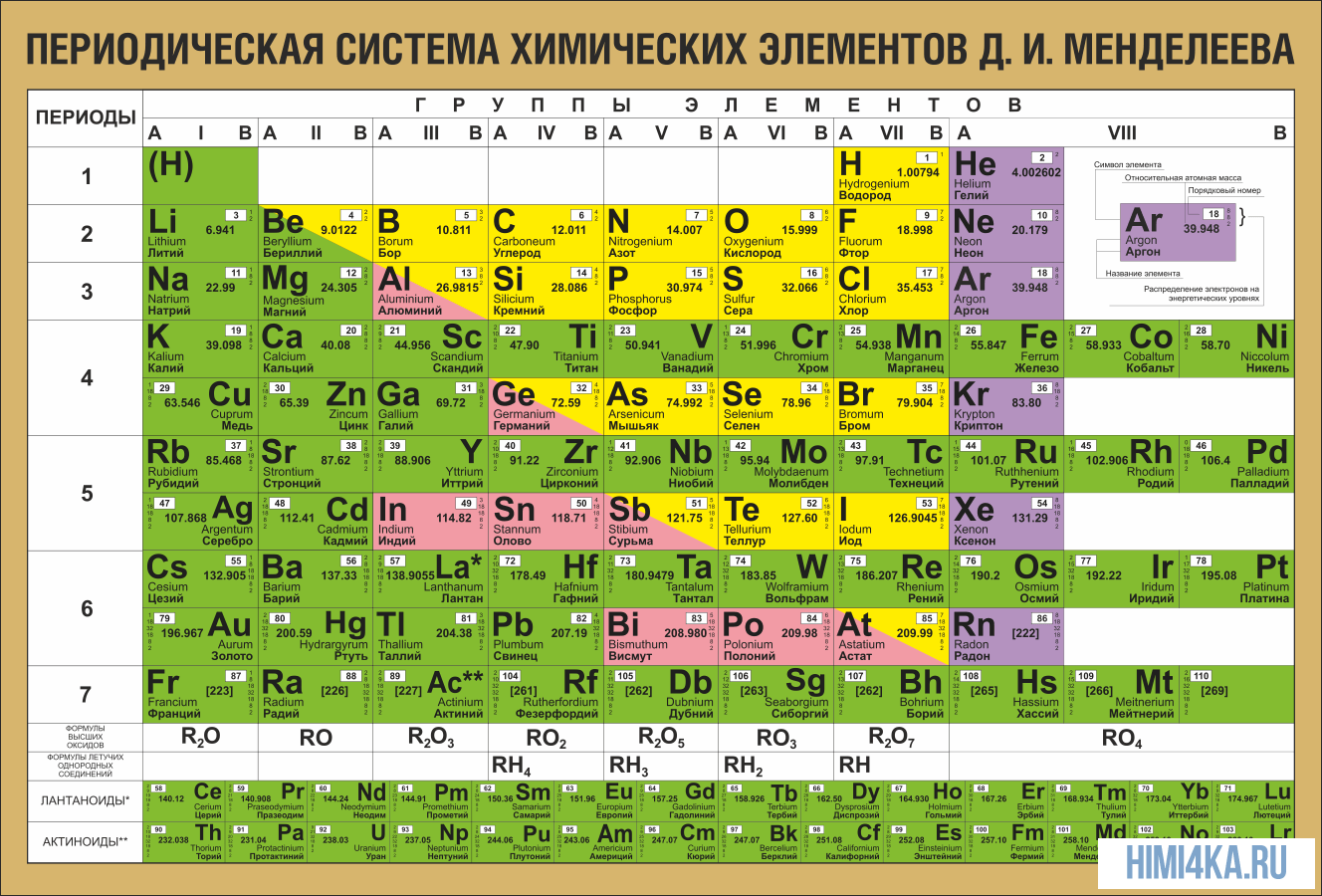
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
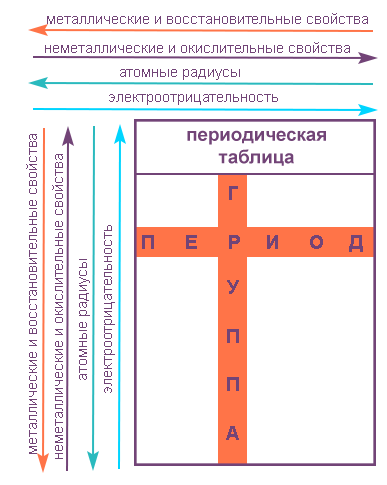
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Хотите ещё проще? Мы создали новый курс, где максимум за 7 дней вы овладете химией с нуля. Подробннее по ссылке
Ядро атома. Ещё раз о причине периодичности.
Ядро атома. Ещё раз о причине периодичности и природе заряда.
Кое-что о природе заряда ядра говорит известный закон английского учёного Генри Мозли (1913 г.). Закон Мозли прост: частота характеристического рентгеновского излучения химического элемента есть линейная функция его порядкового номера (Z). Порядковый номер элемента соответствует заряду ядра элемента, иначе, количеству протонов в ядре атома элемента. Однако в ядре атома есть не только протоны, но и нейтроны, частицы без заряда. Количество протонов и нейтронов в ядре примерно равно. Так что заряд ядра равен половине массы ядра. В рентгеновском аппарате на видео происходит вот что. Ускоренные электроны в поле электрического потенциала в 35 тысяч вольт бьют с большой силой в антикатод, сделанный из трёх разных элементов: железа, меди и молибдена (по очереди). Возникает тормозное рентгеновское излучение сплошного спектра. При большой энергии электронов возникает не только сплошной спектр рентгеновского излучения, но и характеристическое излучение в виде пиков, максимумов. Но, чтобы увидеть такую картинку, излучение должно пройти через дифракционную решетку кристалла, который поворачивается на угол в 30 градусов. Волны излучения огибают узлы решетки кристалла под разными углами, образуя общую картину спектра. Для каждых атомов химических элементов пики на шкале частот излучения свои, единственные. Чем тяжелее ядро атома – тем короче длина излучаемых волн, больше их энергия.
Принято считать, что энергичные электроны выбивают электроны у атомов элементов антикатода, выбивают из ближних к ядру электронных оболочек К и L. Опустевшее место занимают электроны с верхних оболочек, испуская рентгеновские фотоны. На самом деле картина не так проста и понятна. Сомнение вызывает само существование электронных оболочек вокруг ядра атома. Дело в том, что и само ядро атома имеет оболочечную структуру. Частицы ядра тоже располагаются в определённой последовательности, своим порядком. Никакого хаоса в движении ядерных частиц нет. Получается так, что природа продублировала структуру ядер и структуру электронных оболочек, пусть не совсем в точности, но всё же. Прежний опыт нам говорит, что на дублирование такого рода природа скупа, и вряд ли будет здесь повторяться. В действительности мы имеем дело только с ядрами и волновыми полями вокруг ядер. Вся масса атома сосредоточена в ядре (99,9%), и сомнительно, чтобы лёгкие электроны отвечали за все физические и химические особенности атомов. В формуле закона Мозли, совсем без ущерба для главной идеи, можно величину Z заменить величиной массы ядра. И тогда характеристическая частота рентгеновского излучения будет линейной функцией массы элемента (массы ядра). Это даже ближе к мысли Д. И. Менделеева, ведь изначально он строил свою Периодическую систему элементов по возрастанию атомных масс (весов). И формула Мозли будет выглядеть более соответственно: частота характеристического рентгеновского излучения (энергия фотона) пропорциональна массе (полной энергии) ядра.
Закон Мозли говорит о линейности, о строгой последовательности появления характеристических рентгеновских частот. Никакой периодической зависимости, периодической изменчивости тут не наблюдается. Получается так, что заряд ядра вовсе не связан с явлением периодичности, с периодической повторяемостью свойств элементов. С периодичностью связана другая особенность ядра – особенность структуры, строение ядра и характер движения частиц ядра. Периодически изменяется (с последовательным прибавлением частиц) характер их движения, и периодически изменяются физические и химические свойства элементов. Свойства элементов связаны с устойчивостью, с симметричностью или асимметричностью динамических комбинаций ядерных частиц (нуклонов). А уж устойчивость, симметричность и асимметричность системы определяются периодическим характером движения самих частиц и периодическим механизмом их связи. Закон Мозли лишь чётко указывает на прямой рост энергии ядер с ростом их массы. Чем массивнее, тяжелее ядра, тем с большими энергиями движутся их частицы, с большей частотой вращаются в своих ядерных оболочках.
Извините, коли речь зашла о природе атомного ядра и причине периодичности, то мне надо вспомнить мою давнюю научную идею, изображаемую спиральным вариантом Периодической системы химических элементов Менделеева. Не буду теорию излагать здесь целиком, лишь отмечу главный принцип. А именно, решающее значение в ядерной связи частиц, в динамической устойчивости частиц в ядерной оболочке имеет их значение угловых моментов в Пи радианах. Все устойчивые ядерные оболочки имеют в сумме угловой момент (момент вращения), кратный 2Пи, иначе, принцип целочисленности волн де Бройля. Нарушение целочисленности, симметричности структуры ядерной оболочки ведёт к появлению у атома тех или иных свойств, к появлению способности вступать в связь с другими элементами. Интересен механизм того, как атом одного элемента вступает в крепкую связь с атомом или атомами других элементов, где тут «зацепки», «крючки»… Сегодня связь между атомами объясняют взаимодействием статических электрических зарядов. Связь делят на ионную, ковалентную, металлическую. Атомы либо отдают свой отрицательный заряд, либо получают, либо обобществляют, лишь бы в итоге иметь устойчивую конфигурацию внешней оболочки благородных газов с минимумом энергии. Вникать в проблему природы этого самого электрического заряда никому не хочется, заряды есть – и ладно! С этим «мусором под ковром» мы пережили весь двадцатый век и с ним же вошли в двадцать первый. Хотя всем разумным людям понятно, что никакого статического поля электрического заряда нет. Поля есть, но они представляют собой поля беспрерывного кручения, вращения. Левый винт кручения, условно говоря, соответствует заряду плюс, правый винт – минус. Отвечает за появление этих самых зарядов круговое вращение протона. Протон, являясь симметричным радиальным колебанием среды вакуума (дыхание вакуума), способен, как целое, двигаться поступательно и вращательно, образуя тор, кольцо. Вот это кольцо и есть диполь, магнетон, основа всякого атома, ядра атома.
С какой бы скоростью в заполненной ядерной оболочке ни вращался протон в круговом движении, и с каким бы радиусом, но его угловой момент вращения в любой момент времени будет всегда кратен 1/4 Пи радиан. В сумме все вращающиеся протоны в устойчивой заполненной ядерной оболочке дают величину углового момента 2Пи. В Периодической системе (спиральный вариант) у элементов первой, второй и третьей группы в движении ядерных частиц наблюдается асинхронность, что тождественно здесь со смещённой синхронностью. Причина – опережение фазы углового момента на величину, кратную 1/4 Пи. Дополнительные прибавляющиеся частицы вносят в согласованное движение частиц ядерной оболочки смещение фазы углового момента. У элементов первой группы – на 1/4 Пи, у элементов второй группы – на 1/2 Пи, у элементов третьей группы – на 3/4 Пи. Четвертая группа системы элементов – водораздел, отделяющая так называемые электроположительные элементы от электроотрицательных элементов. Элементы четвёртой группы углерода (Пи) могут быть и электроположительными, и электроотрицательными. Элементы пятой (5/4 Пи), шестой (3/2 Пи) и седьмой (7/4 Пи) группы системы являются электроотрицательными, потому что охотно прибирают себе электроны элементов первых трёх групп. В движении частиц ядер элементов 5, 6 и 7 групп системы происходит запаздывание фазы углового момента, что тоже вызывает асинхронность общего движения ядерных частиц. Асинхронность с обратным знаком. Как видите, электроположительность и электроотрицательность объясняются здесь лишь смещением фазы углов орбитальных моментов вращающихся протонов. Соединение «электроотрицательных» элементов с «электроположительными» обусловлено явлением синхронизации. Асинхронность движения ядерных частиц элемента с опережающей фазой углового момента соединяется с асинхронностью элемента с запаздывающей фазой углового момента и получается синхронность, согласование, гармония в общем движении частиц, целочисленность Пи радиан. Пример: молекула поваренной соли, связь атома натрия с атомом хлора. Ядро атома натрия – опережающая асинхронность фазы 1/4 Пи. Ядро атома хлора – запаздывающая асинхронность фазы 7/4 Пи. В сумме две асинхронности дают синхронность 2Пи. Другой пример, более сложный, где связь образуют как бы два элемента запаздывающей фазы – молекула воды: атом кислорода (6/4 Пи) и два атома водорода (7/4 Пи). Дело в том, что водород ярко проявляет двойственные свойства: и щелочных металлов (1 группа), и галогенов (7 группа). Ядро атома кислорода – запаздывающая асинхронность фазы 6/4 Пи. Два ядра атома водорода – в сумме запаздывающая асинхронность фазы 14/4 Пи. В итоге – 5 Пи. Когда же водород идёт опережающей асинхронностью фазы первой группы, то итог суммы – 2 Пи. То есть, несмотря на простоту трактовки – тут не всё так просто и однозначно. Позвольте на этом остановиться. Гипотеза очерчена достаточно.
Вот так, с Божьей помощью, мы сможем со временем преодолеть зарядовый мистицизм. Ведь надо, наконец, выметать сор из-под ковра и наводить тут элементарный порядок. Ведь стыдно, на дворе – двадцать первый век, а мы до сих пор используем представления и образы восемнадцатого века! Ломоносов не побоялся изгнать теплород из научного обихода. А нам-то что мешает изгнать давно устаревшее представление об электрическом заряде?! Да, привыкли, удобно, просто, без затей… Плюс и минус – притягиваются; Плюс и плюс – отталкиваются. Красота! Мир частиц, атомов – это мир колебаний и периодических движений. Так и надо искать такие особенности периодических движений, которые наглядно и непротиворечиво давали бы нам понимание законов этого мира, в том числе – природу заряда.